Documento de consenso sobre la profilaxis posexposición ocupacional y no ocupacional al VIH, VHB y VHC en adultos y niños.
Actualización 2025
Notas de la Versión:
COMITÉ DE REDACCIÓN (por orden alfabético):
Grupo de estudio de SIDA (GeSIDA) y grupo de estudio de hepatitis víricas (GEHEP) de la sociedad española de enfermedades infecciosas y microbiología clínica (SEIMC), el grupo de estudio de infectología pediátrica de la Sociedad española de Pediatría y la Sociedad Española de Medicina Preventiva, Salud Pública y Gestión Sanitaria (SEMPSPGS)
Coordinadores:
- Pablo Bachiller Luque, Unidad de Enfermedades Infecciosas, Servicio de Medicina Interna, Hospital Universitario Río Hortega, Valladolid.
- Carlos Galera Peñaranda, Unidad VIH e ITS, Servicio de Medicina Interna, Hospital Universitario Virgen de la Arrixaca, Instituto Murciano de Investigación Biosanitaria Pascual Parrilla (IMIB), Murcia.
Redactores/as:
- Jésica Abadía Otero, Unidad de Enfermedades Infecciosas, Servicio de Medicina Interna, Hospital Universitario Río Hortega, Valladolid.
- Arantxa Berzosa Sanchez, Servicio de Pediatría, Hospital Clínico San Carlos. Madrid. IdISSC. CIBERINFECC.
- Otilia Bisbal Pardo, Unidad de VIH. Hospital Universitario 12 de Octubre, Madrid. CIBERINFECC.
- Anaïs Corma Gómez. Unidad de Enfermedades Infecciosas y Microbiología, Hospital Universitario de Valme. Instituto de Biomedicina de Sevilla (IBiS). CIBERINFEC.
- Diana Corona Mata. Hospital Universitario Reina Sofía, Córdoba. IMIBIC. CIBERINFEC.
- Alberto Díaz Santiago, Hospital Universitario Puerta de Hierro - Majadahonda, Madrid.
- Julián Manuel Domínguez Fernández, Servicio de Medicina Preventiva, Hospital Universitario de Ceuta.
- Antonio Fernández Quiroga, Servicio de Medicina Preventiva, Hospital Universitario Lucus Augusti, Lugo.
- Juan Flores Cid, Hospital Arnau de Vilanova, Valencia.
- Jesús García Guerrero, Servicio de Medicina Preventiva. Complejo Hospitalario Universitario de Albacete.
- Jorge Néstor García Pérez, Hospital Vall d'Hebron, Barcelona.
- Leire Gil Alonso, Hospital Universitario Donostia, San Sebastián.
- Alexy Inciarte Portillo, Hospital Clinic, Barcelona.
- Montserrat Laguno Centeno. Unidad de VIH. Hospital Clínic de Barcelona. IDIBAPS. CIBERINFEC.
- Raquel Monsalvo Arroyo, Hospital Universitario del Tajo, Madrid.
- Gregorio Montes Salas. Departamento. CC. Biomédicas, Facultad de Medicina y CC. Salud, Universidad de Extremadura. Servicio de Medicina Preventiva, Hospital Universitario de Badajoz.
- Marisa Navarro Gómez. Hospital Gregorio Marañón, CIBERINFEC ISCIII, IISGM, UCM Madrid.
- María Dolores Ocete Mochón, Consorcio Hospital General Universitario, Valencia.
- Inés Pérez Camacho, Hospital Regional Universitario de Málaga, IBIMA.
- Gabriel Reina González, Clínica Universidad de Navarra-Instituto de Investigación Sanitaria de Navarra (IdiSNA), Pamplona.
- Marta Rosas Cancio-Suarez. Servicio de Enfermedades Infecciosas. Hospital Universitario Ramón y Cajal. CIBERINFEC. Madrid.
- Francisco Rubio Osuna. Servicio de Medicina Preventiva y Salud Pública. Hospital Universitario Reina Sofía. Córdoba.
- Alejandro Salinas Botrán, Servicio de Medicina Interna, Hospital Clínico San Carlos, Madrid.
- Ignacio de los Santos Gil. Servicio de Medicina Interna-Infecciosas. Hospital Universitario de la Princesa. CIBERINFEC. Madrid.
- María Velasco Arribas, Hospital Universitario Fundación Alcorcón, Madrid.
- María Jesús Vivancos Gallego, Unidad de VIH. Servicio de Enfermedades Infecciosas. Hospital Universitario Ramón y Cajal, Madrid. CIBERINFEC.
Revisores/a:
- María José Galindo Puerto. Hospital Clínico Universitario, Valencia.
- Federico García García. Hospital Universitario San Cecilio-Instituto de Investigación Biosanitaria, IBS-Granada. CIBERINFEC.
- Arkaitz Imaz Vacas, Hospital Universitari de Bellvitge, L´Hospitalet de Llobregat, Barcelona.
- Luz Martín Carbonero, Hospital La Paz, Madrid.
- Antonio Rivero Román. Hospital Universitario Reina Sofía, Córdoba. IMIBIC. CIBERINFEC.
AGRADECIMIENTOS
Raúl López Izquierdo; Julia Gómez Barquero; Javier Arroyo Fernández; Laura Melero Guijarro; Jesús Álvarez Manzanares; Asunción Díaz Franco; Manuela Zaidan Rodrigues; Beatriz Pérez-Monte; María Teresa Filigeddu; Hortensia Álvarez; Jesús Santos González; Rosario Palacios Muñoz; Rosa María Martínez Álvarez; Fernando Chacón; Imma Clotet; Manuel Cotarelo; Laura Martín, Enrique Vacas y Manuel Vélez Díaz-Pallares.
Cita sugerida:
Grupo de estudio de SIDA (GeSIDA) y grupo de estudio de hepatitis víricas (GEHEP) de la sociedad española de enfermedades infecciosas y microbiología clínica (SEIMC), grupo de estudio de infectología pediátrica de la Sociedad española de Pediatría y Sociedad Española de Medicina Preventiva, Salud Pública y Gestión Sanitaria (SEMPSPGS). Documento de consenso sobre la profilaxis posexposición ocupacional y no ocupacional al VIH, VHB y VHC en adultos y niños. Actualización 2025. [https://guiasclinicas.gesida-seimc.org/]
ABREVIATURAS
3TC Lamivudina
ADD Antivirales de acción directa
Ag p24 Antígeno p24
ANRS l'Agence nationale de recherches sur le sida de Francia
anti-HBc Anticuerpos frente a las proteínas del core del VHB
anti-HBe Anticuerpos frente al antígeno e del VHB
anti-HBs Anticuerpos frente al antígeno de superficie del VHB
anti-VHC Anticuerpos frente al VHC
anti-VIH Anticuerpos frente al VIH
ARN Ácido ribonucleico
ASHM Australasian Society for HIV, Viral Hepatitis and Sexual Health Medicine's
BASHH British Association for Sexual Health and HIV
BIC Bictegravir
CDC Centers for Disease Control and Prevention
CIS Centro de investigaciones sociológicas
CNS Conseil National du Sida et des hépatites virales de Francia
ClCr Aclaramiento de creatinina
cp Cápsula, comprimido
Cr Creatinina
CROI Conference on Retroviruses and Opportunistic Infections
CV Carga viral
DOR Doravirina
DRV Darunavir
DRV / c Darunavir / cobicistat
DTG Dolutegravir
IDSA Infectious Diseases Society of America
ELISA Enzimoinmunoanálisis
ENO Exposición no ocupacional
EO Exposición ocupacional
FTC Emtricitabina
GPT ALT - Alanina aminotransferasa
GBHSH Hombres gais, bisexuales y otros hombres que tienen sexo con hombres
GEHEP Grupo de Estudio de las Hepatitis Víricas de la SEIMC
GeSIDA Grupo de Estudio del SIDA de la SEIMC
HBeAg Antígeno e del VHB
HBsAg Antígeno de superficie del VHB
HSH Hombres que tienen sexo con hombres
IM Intramuscular
IC Intervalo de confianza
IGHB Inmunoglobulina frente al VHB
INE Instituto nacional de estadística
ITS Infecciones de transmisión sexual
LCR Líquido cefalorraquídeo
MIE Maladies infectieuses émergentes de Francia
OR Odds ratio
p.e. por ejemplo
PPE Profilaxis posexposición
PrEP Profilaxis pre-exposición
PVVIH Personas que viven con el VIH
RAL Raltegravir
RTV Ritonavir
RPV Rilpivirina
SEIMC Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica
SEIP Grupo de Infectología de la Sociedad Española de Infectología Pediátrica
SEMPSPGS Sociedad Española de Medicina Preventiva, Salud Pública y Gestión Sanitaria
SIDA Síndrome de la inmunodeficiencia adquirida
TAF Tenofovir alafenamida
TAR Tratamiento antirretroviral
TDF Tenofovir disoproxil fumarato
UDI Usuarios de drogas inyectadas
VHA Virus de la hepatitis A
VHB Virus de la hepatitis B
VHC Virus de la hepatitis C
VHD Virus de la hepatitis D
VIH Virus de la inmunodeficiencia humana
ZDV Zidovudina
DECLARACIÓN DE TRANSPARENCIA (Conflictos de interés)
- Pablo Bachiller Luque, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en los laboratorios Janssen pharmaceuticals; ha recibido compensación económica por charlas de Gilead Sciences, ViiV Healthcare, MSD y Janssen pharmaceuticals, y ayudas en programas de formación o asistencias a reuniones científicas de Gilead Sciences, ViiV Healthcare, MSD y Janssen pharmaceuticals.
- Carlos Galera Peñaranda, no tiene ningún conflicto de interés que declarar en relación con las Guías de PPE.
Redactores/as:
- Jésica Abadía Otero, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener conflicto de intereses.
- Arantxa Berzosa Sánchez, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener conflicto de intereses.
- Otilia Bisbal Pardo, ha recibido ayuda para asistencia a congresos y reuniones científicas y compensación económica por actividades formativas y docentes de Gilead Sciences, Janssen-Cilag, Merck Sharp & Dohme y ViiV Healthcare.
- Anaïs Corma-Gómez, ha recibido honorarios por ponencias de ViiV Healthcare, Johnson & Johnson y Gilead Sciences, y financiación para proyectos de investigación de Gilead Sciences.
- Diana Corona-Mata, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha recibido compensación económica por charlas de GSK-ViiV Healthcare, Gilead Sciences, MSD y Janssen pharmaceuticals.
- Alberto Díaz de Santiago, ha recibido financiación para investigación de Gilead Sciences, ViiV Healthare y Janssen pharmaceuticals. Ha participado en Advisory Boards para Gilead Sciences, ViiV Healthcare, MSD y Janssen pharmaceuticals. Ha recibido compensación económica por charlas de Gilead Sciences, ViiV Healthcare, MSD y Janssen pharmaceuticals.
- Julián Manuel Domínguez Fernández, no ha efectuado labores de consultoría alguna; ni ha recibido compensación económica alguna, ni tiene conflicto de interés alguno.
- Antonio Fernández Quiroga, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener conflicto de intereses.
- Juan Flores Cid, declara haber recibido honorarios por charlas y conferencias de Gilead Sciences, ViiV Healthcare, Janssen Cilag y MSD.
- Jesús García Guerrero, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener conflicto de intereses.
- Jorge Néstor García Pérez, ha recibido remuneración por ponencias docentes por parte de ViiV Healthcare, Janssen pharmaceuticals, MSD y Gilead Sciences.
- Leire Gil Alonso, declara no tener conflicto de intereses para el documento referido.
- Alexy Inciarte Portillo, confirma que no tiene ningún conflicto de interés para el desarrollo de la guía.
- Montserrat Laguno Centeno, ha recibido honorarios por dar charlas, participar en reuniones y/o becas de investigación de las siguientes compañías farmacéuticas: AbbVie, Janssen, MSD, Gilead Sciences y ViiV Healthcare.
- Raquel Monsalvo Arroyo, declara no tener conflicto de intereses para el documento referido.
- Gregorio Montes Salas, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha recibido compensación económica por charlas de GlaxoSmithKline y Pfizer.
- Marisa Navarro Gómez, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en los laboratorios ViiV Healthcare y Pfizer; ha recibido compensación económica por charlas de ViiV Healthcare, Pfizer, MSD y Abbie, así como pagos por desarrollos de presentaciones educacionales para ViiV Healthcare, Pfizer y Abbie.
- María Dolores Ocete Mochón, declara no tener conflicto de intereses para el documento referido.
- Inés Pérez Camacho, declara no tener conflicto de intereses para el documento referido.
- Gabriel Reina González, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en Cinfa, ha recibido becas de investigación de Roche Diagnostics, ayudas para asistencia a Congresos de Vircell y ha participado en actividades educativas, charlas o simposios patrocinados por Qiagen, Roche Diagnostics y Gilead Sciences.
- Marta Rosas Cancio-Suárez, declara haber recibido compensación económica por charlas médicas financiadas por ViiV Healthcare, así como apoyo no financiero de ViiV Healthcare, Janssen Cilag y Gilead Sciences.
- Francisco Rubio Osuna, declara no tener conflictos de interés ni haber realizado labores de consultoría o recibido compensación económica por charlas de ninguna entidad.
- Alejandro Salinas Botrán, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener conflicto de intereses.
- Ignacio de los Santos Gil, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en el laboratorio Janssen; ha recibido compensación económica por charlas de ViiV Healthcare, Janssen y Gilead Sciences, así como pagos por desarrollos de presentaciones educacionales para ViiV Healthcare, Janssen y Gilead Sciences.
- María Velasco Arribas, ha recibido honorarios y/o ayudas para actividades con fines docentes o ponencias de Gilead Sciences, Janssen Cilag, Merck Sharp & Dohme y ViiV Healthcare.
- María Jesús Vivancos Gallego, declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha impartido presentaciones con fines docentes de AbbVie, Gilead Sciences y ViiV Healthcare por las que ha recibido compensación económica, y ha asistido de forma esporádica a congresos con la financiación de Gilead Sciences, ViiV Healthcare y Janssen Cilag.
Revisores/a:
- María José Galindo Puerto, ha recibido honorarios de ViiV Healthcare, Johnson & Johnson, MSD y Gilead Sciences por realizar presentaciones, materiales educativos y asesorías.
- Federico García García, ha recibido ayudas para proyectos de investigación de Gilead Sciences, ViiV Healthcare, MSD y Roche; honorarios por ponencias de ViiV Healthcare, Gilead Sciences, AbbVie, MSD, Janssen, Roche, Biomerieux, Hologic, Qiagen; ha recibido ayudas para asistencia a actividades formativas de ViiV Healthcare, Gilead Sciences, AbbVie, MSD, Janssen, Roche, Biomerieux, Hologic, Qiagen; y ha realizado labores de asesoramiento para ViiV Healthcare, Gilead Sciences, AbbVie, Roche y Hologic.
- Arkaitz Imaz Vacas, ha recibido compensación económica por charlas, actividades formativas y/o participación en consultorías, así como becas para investigación y ayudas para asistencia a congresos científicos de Gilead Sciences, Johnson & Johnson, Merck Sharp & Dohme, TheraTechnologies y ViiV Healthcare.
- Luz Martín Carbonero, ha efectuado labores de consultoría para ViiV Healthcare y Gilead Sciences. Ha recibido compensaciones económicas por charlas de Gilead Sciences, Janssen y ViiV Healthcare. Ha recibido igualmente ayudas económicas para asistir a reuniones científicas de Gilead Sciences.
- Antonio Rivero Román o su institución, han recibido fondos para formación, investigación u honorarios profesionales de ViiV Healthcare, MSD, Janssen, AbbVie y Gilead Sciences.
1. INTRODUCCIÓN
Presentación, justificación y objetivos
La Profilaxis posexposición (PPE) al virus de la Inmunodeficiencia Humana (VIH), virus de la Hepatitis B (VHB) y virus de la Hepatitis C (VHC), es una estrategia de intervención biomédica dirigida a prevenir la transmisión de estos virus en personas expuestas, generalmente de forma excepcional y esporádica, cuando la prevención primaria ha fallado.
Este documento es una revisión y actualización del documento previo publicado en 2015 por varias sociedades científicas y grupos de estudios coordinados desde el Plan Nacional del SIDA 1. El documento está dirigido tanto a profesionales sanitarios directamente implicados en el manejo de la infección por VIH, como aquellos que puedan enfrentarse a esta situación de forma esporádica. En los diferentes capítulos se analizan la prevalencia de estas infecciones, el riesgo de transmisión en diferentes poblaciones, en qué situaciones está indicado el uso de la PPE, qué pautas y recomendaciones se deben seguir de forma preferente y qué seguimiento debemos realizar para alcanzar la máxima eficacia y minimizar los efectos secundarios. En esta nueva edición hemos incluido un capítulo sobre PPE en niños y adolescentes, un capítulo sobre PPE en situaciones especiales, otro de las novedades respecto a las guías anteriores, y finalmente uno que incluye aquellas situaciones donde no se recomienda actualmente el uso de PPE.
Hemos querido realizar un documento práctico y de fácil manejo, incluyendo tablas y algoritmos para simplificar la lectura sobre el manejo de la PPE. Sin embargo, algunos capítulos, relacionados con aspectos de la PPE en los que existe un mayor grado de incertidumbre o controversias, han sido elaborados de forma más extensa. Estas guías sobre PPE pretenden ser un documento de apoyo en la toma de decisiones, pero en ningún caso sustituye al criterio final del clínico, en base a un análisis individualizado de cada caso. En el ánimo de los promotores y redactores de este documento está la revisión continúa de la evidencia para poder ofrecer nuevas actualizaciones.
Metodología
Se ha constituido un grupo de redactores, expertos en el campo de la infección por VIH y las hepatitis víricas, pertenecientes al Grupo de Estudio del SIDA (GESIDA) y al Grupo de Estudio de las Hepatitis Víricas (GEHEP) de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC), a la Sociedad Española de Infectología Pediátrica (SEIP) y a la Sociedad Española de Medicina Preventiva, Salud Pública y Gestión Sanitaria (SEMPSPGS). El trabajo ha sido coordinado desde SEIMC por dos coordinadores (un coordinador de GESIDA y otro de GEHEP). Todos los participantes en la elaboración del documento lo han hecho de forma altruista y han firmado un documento declarando sus conflictos de intereses.
Los diferentes capítulos han sido elaborados por los redactores responsables de cada uno de ellos. La elaboración de cada uno de los capítulos se ha realizado tras una búsqueda bibliográfica en las bases de datos más habituales (Medline, Pubmed, UpToDate, Web of Science, Registro Cochrane y MD Consult), hasta la fecha de 31 de octubre de 2024. Además se han revisado las Guías sobre PPE publicadas por GESIDA 1, por los CDC 2, la British Association for Sexual Health and HIV (BASHH) 3, las Guías de la Australasian Society for HIV, Viral Hepatitis and Sexual Health Medicine's (ASHM) 4, las Guías de Tratamiento preventivo postexposición al VIH elaboradas por Conseil National du Sida et des hépatites virales (CNS) et l'Agence nationale de recherches sur le sida | Maladies infectieuses émergentes (ANRS | MIE) de Francia 5, y la guía Post-Exposure Prophylaxis (PEP) to Prevent HIV Infection, actualizada el 3 de octubre de 2024 por el New York State Department of Health and AIDS Institute Guideline 6. Por último, también se han revisado las comunicaciones sobre PPE presentadas en el congreso CROI los años 2020-2024.
Tras su elaboración, los capítulos han sido revisados por un equipo de 5 revisores. Finalmente, los coordinadores han elaborado un primer borrador, que ha sido sometido a la revisión, en primer lugar, de todos los miembros del panel y posteriormente, tras incorporar las correcciones o sugerencias consensuadas, fue expuesto de forma pública en las web de las sociedades y grupos de estudio participantes.
Para la graduación de las recomendaciones y la valoración de la calidad de la evidencia que las sustentan se ha utilizado una modificación de los criterios de la Infectious Diseases Society of America (IDSA). En la siguiente Tabla 1 se resumen los criterios.
Tablas:

Bibliografía:
Panel de Expertos de GeSIDA. Documento de consenso sobre profilaxis postexposición ocupacional y no ocupacional en relación con el VIH, VHB y VHC en adultos y niños. (actualización marzo 2015). Accesible en: https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/hepatitisC/informacion/docs/Profilaxis_postexposicion_ocupacional_y_no_ocupacional_VIH_VHB_VHC(PPE).pdf
Centre for Disease Control. Updated Guidelines for Antiretroviral Postexposure Prophylaxis after Sexual, Injection-Drug Use, or Other Nonoccupational Exposure to HIV - United States, 2016. MMWR Morb Mortal Wkly Rep. 2016 May 6;65(17):458. doi: 10.15585/mmwr.mm6517a5. PMID: 27149423. https://stacks.cdc.gov/view/cdc/38856
Cresswell F, Asanati K, Bhagani S, Boffito M, Delpech V, Ellis J, et al. UK guideline for the use of HIV post-exposure prophylaxis 2021. HIV Med. 2022 May;23(5):494-545. doi: 10.1111/hiv.13208. Epub 2022 Feb 14. Erratum in: HIV Med. 2022 Jul;23(6):701. PMID: 35166004. Accesible en https://onlinelibrary.wiley.com/doi/epdf/10.1111/hiv.13208
Australasian Society for HIV, Viral Hepatitis and Sexual Health Medicine's (ASHM). National guidelines for post-exposure prophylaxis after non-occupational and occupational exposure to HIV 2023. Accesible en: https://pepguidelines1.wpenginepowered.com
Le Conseil National du Sida et des hépatites virales (CNS) et l'Agence nationale de recherches sur le sida | Maladies infectieuses émergentes (ANRS | MIE). Traitement préventif post-exposition au VIH. Practice guidelines - Updated on Aug 02 2024. Accesible en: https://www.has-sante.fr/jcms/p_3536535/en/traitement-preventif-post-exposition-au-vih#voirAussi
New York State Department of Health and AIDS Institute Guideline. Post-Exposure Prophylaxis (PEP) to Prevent HIV Infection. Actualización 3 de octubre de 2024. Accesible en: https://www.hivguidelines.org/guideline/hiv-pep/?mycollection=pep-prep
2. DEFINICIONES Y CONCEPTOS
Las siguientes definiciones pretenden facilitar la comprensión de los términos incluidos en el presente Documento de una manera clara, concisa y concreta. En el mismo se hace referencia únicamente a los siguientes virus de transmisión por vía sanguínea o sexual: VIH, VHB y VHC.
Todos los conceptos son válidos tanto en el ámbito hospitalario como extrahospitalario y son aplicables tanto a adultos como a niños.
Los aspectos relativos a responsabilidad legal y otras contingencias referentes a salud laboral no son objeto del presente Documento, dependiendo de la normativa vigente establecida en cada caso.
Accidente biológico: evento no deseado que se produce al contactar con un líquido biológico por vía parenteral, por lesión percutánea, salpicadura sobre piel no intacta o exposición a mucosas (boca, ojos, vagina o recto).
Chemsex 1: uso intencionado de drogas para tener relaciones sexuales por un período largo de tiempo (que puede durar varias horas hasta varios días) predominantemente entre hombres gais, bisexuales y otros hombres que tienen sexo con hombres (GBHSH).
Exposición no ocupacional: aquella que ocurre a consecuencia del contacto con sangre u otro líquido biológico potencialmente infeccioso fuera del ámbito laboral, incluyendo la exposición sexual sin protección, la exposición percutánea en usuarios de drogas por vía parenteral, los pinchazos accidentales y las mordeduras humanas.
Exposición ocupacional: aquella que ocurre a consecuencia de la realización de un trabajo donde se contacta con sangre u otro líquido biológico potencialmente infeccioso, pudiendo suponer un riesgo de infección para el trabajador sanitario.
Fluidos potencialmente infecciosos: se incluyen sangre, semen, secreciones vaginales, leche materna y otros líquidos biológicos (líquido cefalorraquídeo, pericárdico, pleural, peritoneal, sinovial y amniótico). No incluidos otros líquidos biológicos como: el sudor, saliva, lágrimas, orina, heces, vómitos o secreciones respiratorias salvo que contengan sangre visible.
Fuente: persona, objeto o líquido biológico desde la cual el agente infeccioso puede transmitirse a la persona expuesta.
Persona expuesta: cualquier persona que sufre contacto con un líquido biológico procedente de una fuente potencialmente infectada por un agente infeccioso.
Profilaxis posexposición (PPE) 2: estrategia de prevención biomédica que se inicia después de la exposición a un patógeno para evitar el desarrollo de una infección.
Profilaxis preexposición (PrEP) 3: intervención biomédica basada en fármacos antirretrovirales dirigida a prevenir la transmisión del VIH en personas seronegativas con alto riesgo de contraer la infección.
Slam, slamsex o slamming 1: término utilizado para referirse al consumo inyectado de drogas en el contexto de chemsex.
Trabajador sanitario: profesional de la salud con los conocimientos y habilidades necesarios para el desarrollo de actividades de tratamiento, cuidado de individuos o manipulación de sustancias biológicas.
Virus de transmisión parenteral: aquellos que pueden estar presentes en la sangre humana y otros líquidos biológicos capaces de producir enfermedad en humanos. Dentro de estos agentes se incluyen el VIH, VHB y VHC.
Bibliografía:
Secretaría del Plan Nacional sobre el Sida. Ministerio de Sanidad. 2020. Documento técnico sobre abordaje del fenómeno del chemsex. Accesible en: https://www.sanidad.gob.es/ca/ciudadanos/enfLesiones/enfTransmisibles/sida/chemSex/docs/DocumentoDEF.pdf Consultado 03/2024
Panel de Expertos de GeSIDA. Documento de consenso sobre profilaxis postexposición ocupacional y no ocupacional en relación con el VIH, VHB y VHC en adultos y niños (marzo 2015). Accesible en: https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/hepatitisC/informacion/docs/Profilaxis_postexposicion_ocupacional_y_no_ocupacional_VIH_VHB_VHC(PPE).pdf Consultado 03/2024.
GeSIDA. Recomendaciones sobre la Profilaxis Pre-Exposición para la Prevención de la Infección por VIH en España (marzo 2023). Accesible en: https://gesida-seimc.org/wp-content/uploads/2023/03/Guia-profilaxis.pdf
3. NOVEDADES RESPECTO A LAS GUÍAS PREVIAS
- Respecto a la estructura de las Guías, se ha introducido un capítulo de PPE en situaciones especiales y un capítulo que recoge las situaciones donde no está recomendado de forma general el uso de PPE.
- En la exposición ocupacional al VIH, se considera que, tras un accidente de riesgo con exposición a fluidos corporales de un paciente con VIH y carga viral plasmática indetectable, la posibilidad de transmisión del VIH es prácticamente nula. No obstante, se debe ofrecer PPE individualizando la decisión, tras diálogo con la persona expuesta.
- Existe evidencia suficiente para afirmar que el riesgo de transmisión del VIH de una PVVIH que recibe TAR y tiene carga viral menor de 200 copias/ml (al menos 6 meses y con buena adherencia), a través de relaciones sexuales sin preservativo es nulo, independientemente del tipo de relación sexual.
- En el capítulo 4, punto 4.3.2 se realiza una aproximación a la prevalencia de VIH en diferentes colectivos en España y una estimación del riesgo de transmisión según el tipo de exposición, basado en datos del Ministerio y de ONUSIDA referentes al año 2022, y tomando como referentes el continuo de atención al VIH de 2024. Se estima que la prevalencia de infección por VIH en España es de 0,2-0,3 %, y que la prevalencia de personas con VIH y carga viral detectable en España es del 0,04-0,06 %.
- Se aporta tabla resumen de indicaciones de uso de PPE según estado de la fuente respecto al VIH, y tipo de exposición (Tema 4, tabla 4.2).
- A lo largo del documento se señala de forma clara que el inicio de la PPE, cuando esté indicada, debe realizarse lo antes posible, idealmente en las primeras 2 horas, preferiblemente en las primeras 12 horas, y siempre antes de las 72 horas.
- Se insiste en la necesidad de valorar la indicación de PPE en aquellas personas que van a iniciar PrEP y hayan tenido una exposición de riesgo en las 72 horas previas. También se insiste en la oportunidad de continuar con PrEP en aquellas personas que se les indica la administración de PPE tras contacto sexual, descartando infección aguda por el VIH mediante un ELISA de 4ª G y/o una PCR VIH al final de la PPE.
- En aquellos usuarios de PrEP con mala adherencia, se valorará ofrecer PPE tras una exposición de riesgo, según el grado de adherencia a la misma. (Tema 5, tabla 5.1)
- Se incluyen las recomendaciones de PPE en el contexto de Chemsex y slamsex, así como en personas en tratamiento frente al VHB.
- Se han actualizado las pautas de PPE consideradas como preferentes, y alternativas (Tema 6, tabla 6.1). También se han ampliado las opciones de PPE en personas embarazadas y en población pediátrica.
- Se han simplificado los análisis de seguimiento en las personas que reciben PPE, y el tiempo estimado para descartar infección por VIH tras la exposición de riesgo se ha reducido a 12 semanas, siempre que se utilice un test diagnóstico de VIH 1-2 de cuarta generación. El seguimiento tras exposición al VHB / VHC dependerá de la situación serológica de la persona fuente y de la persona expuesta, y de la necesidad o no de vacunación frente al VHB.
- Finalmente, se ha tratado de emplear un lenguaje inclusivo, desestigmatizar la toma de PPE en el contexto de relaciones sexuales, y respetar el principio de autonomía de la persona expuesta a la hora de decidir si quiere tomar PPE.
4. EVALUACIÓN DEL RIESGO DE TRANSMISIÓN AL VIH, VHB Y VHC E INDICACIONES DE PPE
4.1. Riesgo y fundamentos
4.2. Evaluación del riesgo de transmisión ocupacional del VIH, VHB y VHC
4.3. Evaluación del riesgo de transmisión no ocupacional del VIH, VHB y VHC
4.4. Evaluación de otras infecciones
4.5. Recomendaciones generales e indicación de PPE ante la exposición ocupacional y no ocupacional frente al VIH, VHB y VHC
Riesgo y fundamentos
Las vías de transmisión del VIH, VHB y VHC incluyen la vía sexual, la exposición a sangre y/o a otros fluidos. No siempre es posible prevenir la exposición de riesgo por lo que la PPE es la única medida preventiva que puede adoptarse una vez que ésta se ha producido.
La probabilidad de que se produzca la infección depende de varios factores: la naturaleza de la exposición, la fuente de exposición, el tipo y duración del contacto, la carga viral de la persona fuente (en el caso del VIH), el estado de vacunación (en el caso del VHB), la presencia de otras infecciones, como por ejemplo las infecciones de transmisión sexual (ITS) y el tiempo transcurrido desde la exposición 1. Con respecto al VIH, se ha demostrado que una vez que el virus atraviesa la barrera mucosa, su replicación no comienza a ser efectiva hasta pasadas las 48 horas. Por este motivo, la PPE frente al VIH tiene más probabilidades de ser eficaz si se inicia idealmente en las primeras dos horas, preferiblemente en las primeras 12 horas, y siempre antes de las 72 horas. La PPE frente al VHB puede iniciarse hasta una semana después de la exposición, aunque lo ideal es hacerlo en las primeras 48 horas. No existe PPE efectiva para prevenir la infección por el VHC por lo que su diagnóstico y tratamiento precoces serán claves para erradicar la infección y prevenir la progresión de la enfermedad.
No existen datos de ensayos clínicos controlados aleatorizados que proporcionen evidencia de la eficacia de la PPE en la prevención de la adquisición del VIH y VHB. En lo que concierne al VIH, los datos en animales han sido especialmente informativos respecto a la importancia de comenzar de forma precoz la PPE, así como acerca de su duración 2. También se ha extrapolado evidencia a partir de datos de transmisión vertical, donde la PPE administrada al recién nacido redujo significativamente el riesgo de adquisición de VIH de madres sin supresión virológica en el momento del parto; y tras exposiciones ocupacionales (EO), donde el riesgo de adquisición de VIH se redujo en general en un 81 % 3. El único estudio observacional en el que se evaluó la eficacia de la PPE para la prevención del VIH tras una exposición no ocupacional (ENO) se realizó entre 200 hombres que tenían sexo con hombres (HSH) en Brasil. Se produjeron 1/68 seroconversiones frente al VIH en el grupo de PPE en comparación con 10/132 en el grupo que no recibió PPE, aunque estos resultados no fueron estadísticamente significativos, probablemente por falta de potencia estadística del estudio 5.
Aunque la PPE es altamente efectiva cuando se inicia de forma precoz y existe una correcta adherencia a la pauta, se han documentado algunas seroconversiones debido, en la gran mayoría de casos, a la persistencia de la conducta / factor de riesgo una vez completada la PPE 6. Otras potenciales causas de fallo de la PPE pueden ser el retraso en el inicio, la adherencia subóptima o la infección primaria precoz ya presente en el momento de iniciar la PPE.
En cualquier caso, el inicio y mantenimiento de la PPE debe estar supeditado a una evaluación exhaustiva y rigurosa de los riesgos asociados con la exposición, con el objetivo de determinar la probabilidad de transmisión viral y la necesidad de instaurar medidas adicionales.
Evaluación del riesgo de transmisión ocupacional del VIH, VHB y VHC
4.2.1. Evaluación del riesgo de transmisión ocupacional del VIH
La PPE para VIH se determina tras una evaluación minuciosa de: 1) tipo de exposición; 2) la persona fuente y 3) la persona expuesta.
Es crucial su rápida asistencia para iniciarla pronto, idealmente en las primeras 2 horas, preferiblemente en las primeras 12 horas, y siempre antes de las 72 horas.
1.-Los tipos de exposición pueden ser:
Exposiciones percutáneas: son más eficientes en la transmisión del VIH que las mucosas. Los CDC estiman que el riesgo promedio de seroconversión del VIH después de una EO percutánea de un caso índice VIH positivo que no recibe TAR supresor es aproximadamente del 0,3 % (IC 95 %: 0,2 a 0,5 %), lo que supone 3 infecciones por cada 1000 incidentes 6. El uso de guantes disminuye el 50 % el volumen inyectado.
Con respecto a los factores relacionados con la exposición percutánea, el riesgo dependerá de:
a.- La profundidad del pinchazo:
- Inoculación superficial: erosión
- Profundidad intermedia: aparición de sangre
- Inoculación profunda (OR 15; IC del 95 %: 6,0 a 41,0) 4.
b.- Tipo de material utilizado:
- Aguja hueca: mayor riesgo que con las agujas de sutura. Este riesgo es proporcional al diámetro de la aguja.
- Aguja maciza o bisturí: menor riesgo que con la anterior
c.- Tipo de fluido al que se ha expuesto el trabajador, siendo el de mayor riesgo la sangre visible en el dispositivo (OR 6,2; IC del 95 %: 2,2 a 21,0) o si ha estado dentro de una arteria o vena 4. Fluidos con elevado potencial infeccioso que requieren evaluación precisa son: la sangre, el semen, las secreciones vaginales y otros fluidos con sangre visible. Podrían ser potencialmente infecciosos el LCR, los líquidos serosos y el líquido amniótico. La exposición a vómito, heces, saliva, sudor, lágrimas, orina y esputo no comporta un riesgo significativo, excepto si contienen sangre visible.
Exposiciones mucocutáneas o lesiones por salpicaduras: se estima que el riesgo de adquirir el VIH a través de una lesión mucocutánea por salpicadura por fluidos con sangre es de alrededor del 0,1 % (1 en 1.000 exposiciones) si la persona fuente VIH no recibe TAR 7.
El VIH no se puede transmitir a través de la piel intacta. El riesgo de transmisión del VIH a través de la piel no intacta (por ejemplo, abrasiones, cortes, heridas) se considera insignificante.
2.- Características de la persona fuente
Es fundamental conocer la situación serológica de la persona fuente contactando con su médico responsable. Si ésta no se sabe o no se puede conocer, se debe realizar un estudio serológico completo siempre que sea posible, previa solicitud de consentimiento verbal o por escrito, con HBsAg, Anti-VHC (si es positivo, medir la carga viral), VIH (si es positivo, medir la carga viral).
Aunque existen interrogantes sobre la persona fuente VIH negativa que podría estar en el período ventana antes de la seroconversión, hasta la fecha no se han registrado casos de transmisión en esta situación. Por lo tanto, no es necesario investigar si una persona fuente pudiera estar en el período ventana para determinar si está indicada la PPE, a menos que se sospeche clínicamente un síndrome retroviral agudo. Las pruebas combinadas de Ag p24 y Ac contra el VIH del ELISA de cuarta generación producen resultados rápidos y precisos, y su detección permite identificar la mayoría de las infecciones durante este período 8. La administración de PPE no debe retrasarse mientras se esperan los resultados de las pruebas. Si se determina que la serología de VIH de la persona fuente es negativa, se debe suspender la PPE y no está indicado realizar pruebas de seguimiento.
En el caso de que la persona fuente tenga infección por el VIH conocida, es fundamental conocer la carga viral, el tipo de TAR (si lo recibe), así como la historia farmacológica y los motivos de cambio de tratamiento (resistencias o intolerancia) 10. Existen varios estudios que demuestran que la exposición a elevadas cargas virales se asocia a mayor riesgo de transmisión de la infección 611. Por este motivo, en los periodos de elevada viremia como son las fases de infección aguda o las fases avanzadas de la enfermedad, si la fuente no está recibiendo TAR, el riesgo de transmisión es mayor 12.
Un accidente de riesgo con exposición a fluidos corporales de un paciente con una carga viral indetectable hace muy improbable la transmisión del VIH. No obstante, se debe ofrecer la PPE individualizando la decisión de inicio y mantenimiento en función de las características del accidente, de los datos analíticos de la fuente y tras diálogo con la persona expuesta.
Si no se puede conocer la situación serológica de la fuente, se valorarán las características clínicas y epidemiológicas y en caso de duda se considerará como de alto riesgo.
- Características de la persona expuesta (trabajador sanitario)
Se debe realizar un estudio serológico completo a la persona expuesta para determinar su estatus serológico frente al VIH, VHB y VHC.
Basándonos en estas 3 características se puede establecer una gradación del riesgo de adquisición del VIH tras una exposición ocupacional:
- Riesgo muy alto: accidente con gran volumen de sangre (pinchazo profundo con aguja usada en acceso vascular del paciente) y persona fuente con alta carga viral plasmática de VIH.
- Riesgo alto: accidente con gran volumen de sangre o con sangre de persona fuente con alta carga viral plasmática de VIH. Se incluyen contactos mucocutáneos con fluidos que también tienen alta carga viral de VIH y que sean: muy prolongados, sobre un área extensa o con piel no íntegra.
- Riesgo bajo: accidente sin exposición a gran volumen de sangre ni procedente de persona con carga viral plasmática de VIH elevada (p. e. pinchazo con aguja de sutura y con carga viral indetectable) 13.
4.2.2. Evaluación del riesgo de transmisión ocupacional del VHB y VHC
El VHB permanece viable e infeccioso durante períodos de hasta 1 semana en las superficies 14 y se transmite de manera eficiente a través de la exposición percutánea o mucosa a sangre o fluidos corporales. El VHC se transmite principalmente a través de la exposición parenteral, con mayor frecuencia a través de agujas contaminadas.
El riesgo de hepatitis B después de un pinchazo con una aguja procedente de un paciente con HBsAg+ es muy superior al riesgo de infección por el VIH: 6-30 % 15 si el trabajador expuesto no está vacunado o, si estando vacunado presenta un título de Anti-HBs < 10 mUI/ml 16.
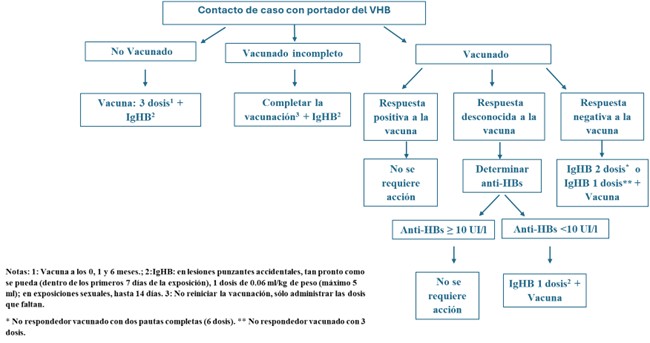
Es fundamental evaluar la presencia de la infección en la persona fuente. Si no se sabe o no se puede conocer, se debe realizar un estudio serológico completo siempre que sea posible, previa solicitud de consentimiento informado verbal o por escrito, con HBsAg, anticuerpos anti-VHC (si es positivo solicitar una carga viral) así como serología de VIH. Además, se debe evaluar la susceptibilidad del trabajador expuesto, conocer su estado inmunológico, vacunación y el título previo de anticuerpos anti HBs. La seroprevalencia en España de HBsAg+ es del 0,22 %, aunque sólo el 0,05 % de la población tiene ADN-VHB detectable en plasma (replicación viral activa). La prevalencia de HBsAg+ es superior en poblaciones clave: 5,3 % en UDI o 3,7 % en PVVIH 17. Para aquellas personas no vacunadas o con estado inmunológico incierto, se debería ofrecer una primera dosis o dosis de recuerdo de la vacuna para el VHB a la espera de los resultados del Anti-HBs. Si se trata de un paciente no vacunado, o con un título de Anti-HBs < 10 UI en el momento de la exposición, se procederá a completar la vacunación del VHB con una pauta rápida (0, 1 y 6 meses). Si la fuente es HBsAg+ se aconseja también administrar una dosis de gammaglobulina específica en las primeras 12 - 24 h tras el contacto. En la Figura 1 se expone el algoritmo de actuación frente a la exposición al VHB.
Según los datos recogidos en un estudio realizado entre 2017-2018 en España, la prevalencia de anticuerpos anti VHC (Anti-VHC) en nuestro medio es del 0,85 % y con viremia activa (ARN-VHC+) sólo el 0,22 %; no obstante, una estimación reciente realizada en el año 2022, reduce esta tasa al 0,12 %. La prevalencia de Anti-VHC es superior en poblaciones clave: 45,9 % en UDI, 9,76 %, en internos en instituciones penitenciarias (0,92 % con ARN-VHC+), 24,4 % en PVVIH (1,7 % con ARN-VHC+), 1,8 % en HSH y 0,4 % en usuarios de PrEP 17. Por lo tanto, se deberá realizar la valoración de la situación serológica de la fuente siempre que se pueda y si esto no es posible, una estimación del riesgo teniendo en cuenta los datos epidemiológicos.
La posibilidad de infección por VHC en personal sanitario tras la EO con agujas se estima que es del 0 al 3 % 18, y la carga viral inoculada es uno de los factores que pueden influir en la probabilidad de adquirir la infección 1920. Así, la incidencia de infección aguda por VHC es baja, (frecuencia de seroconversión según los CDC del 1,8 %) 21. No obstante, es necesario realizar un correcto seguimiento serológico tras el accidente ya que, en la mayoría de los casos, la hepatitis aguda cursa de forma asintomática. No disponemos de vacuna ni existe una profilaxis efectiva frente al VHC, por tanto, es importante el seguimiento estrecho de estas personas para poder diagnosticar cuanto antes la infección e iniciar el tratamiento de forma inmediata 22.
Evaluación del riesgo de transmisión no ocupacional del VIH, VHB y VHC
4.3.1. Evaluación del riesgo de transmisión no ocupacional del VIH
Nos referiremos en este apartado al riesgo de transmisión del VIH a través de relaciones sexuales. En el capítulo 5 se analizan otros tipos de exposición no ocupacional.
La probabilidad de transmisión del VIH dependerá fundamentalmente de:
a.- Tipo de exposición. En el caso de exposición traumática, con violencia, como en relaciones sexuales no consentidas o si se produce sangrado o menstruación, el riesgo se incrementa considerablemente. También cuando ha habido múltiples exposiciones en las últimas 72 horas 2324.
b.- Estado de la persona fuente y la cantidad de virus en el inóculo. No habrá riesgo de transmisión si la fuente es VIH negativa, pero con frecuencia no se conoce el estado de la fuente respecto del VIH; en estos casos la valoración del riesgo debe ser individualizada.
En personas con VIH y enfermedad avanzada (con niveles bajos de CD4, o sida), si la persona fuente no está recibiendo TAR, y durante la infección aguda, la carga viral suele ser muy elevada. En estos casos, el riesgo de transmisión aumenta 2,9 veces 2526.
En una revisión sistemática de la literatura que incluyó 7 762 parejas serodiscordantes en 25 países no se encontró evidencia definitiva de la transmisión del VIH cuando las cargas virales eran inferiores a 600 copias/ml y sucedió de manera extremadamente rara cuando las cargas virales estaban entre 600 - 1000 copias/ml. Además, los estudios de infectividad han demostrado que el riesgo estimado de transmisión por exposición sexual sin preservativo cuando la pareja índice tenía una carga viral de 1000 copias/ml es extremadamente pequeño (0,00028 %) 27.
Existe evidencia suficiente para afirmar que el riesgo de transmisión del VIH de una PVVIH que recibe TAR y tiene carga viral menor de 200 copias/ml, a través de relaciones sexuales sin preservativo, es nulo, independientemente del tipo de relación sexual 28.
- Individuo expuesto. La presencia de lesiones genitales o ITS en el individuo expuesto también son factores que facilitan la infección 29. Por otro lado, la probabilidad de adquisición del VIH por relación sexual es mayor al final del embarazo (riesgo relativo ajustado 2,82, p=0,01) y en el período posparto (3,97, p=0,01) en comparación con la mujer no embarazada 30.
4.3.2. Cálculo individualizado del riesgo de transmisión del VIH
El cálculo del riesgo final de transmisión dependerá de la prevalencia de la infección VIH en la población a la que pertenece la persona fuente, más concretamente de la prevalencia de viremia detectable del VIH en esa población, y del riesgo estimado inherente al tipo de exposición.
Según datos del Ministerio y de ONUSIDA referentes al año 2022, y tomando como referentes el continuo de atención al VIH más reciente, en España hay entre 130 000 y 170 000 PVVIH, prevalencia del 0,2 - 0,3 %, con una fracción no diagnosticada del 7,5 %, lo que supone entre 8 623 y 15 461 personas que desconocen su situación de infección por el VIH. Entre aquellas que están correctamente diagnosticadas, el 96,6 % reciben tratamiento antirretroviral, y de estas el 90,4 % tienen carga viral suprimida 3132. Aplicando estos datos sobre la población española en julio de 2022, 47 615 034 habitantes (Instituto Nacional de Estadística, INE, nota de prensa 18 nov 2022), la prevalencia de personas con VIH y carga viral detectable en la población general en España es del 0,04 - 0,06 %.
No existen datos oficiales de prevalencia de infección por el VIH y de viremia en diferentes poblaciones, no obstante, en base a datos de población del INE, publicaciones del Centro de Investigaciones sociológicas, CIS 33, la Encuesta europea on-line para HSH (EMIS-2017) 34, y el informe del Observatorio Español de la Drogas y las Adicciones 2023 35, hemos realizado una aproximación. Según estos datos, la prevalencia de viremia por VIH (Carga viral > 200 copias/ml) en el colectivo de GBHSH es de 9 personas cada 1000, entre 17 y 32 personas de cada 1000 UDI, y solo 2 cada 10 000 personas entre los hombres y mujeres heterosexuales. La incertidumbre que pueden generar resultados sustentados en distintas presunciones, aún basados en documentos oficiales, aconsejan ser cautos a la hora de aplicarlos, pero nos sirven para valorar que la prevalencia de personas con VIH virémicas, a día de hoy en España, es baja en la mayoría de colectivos.
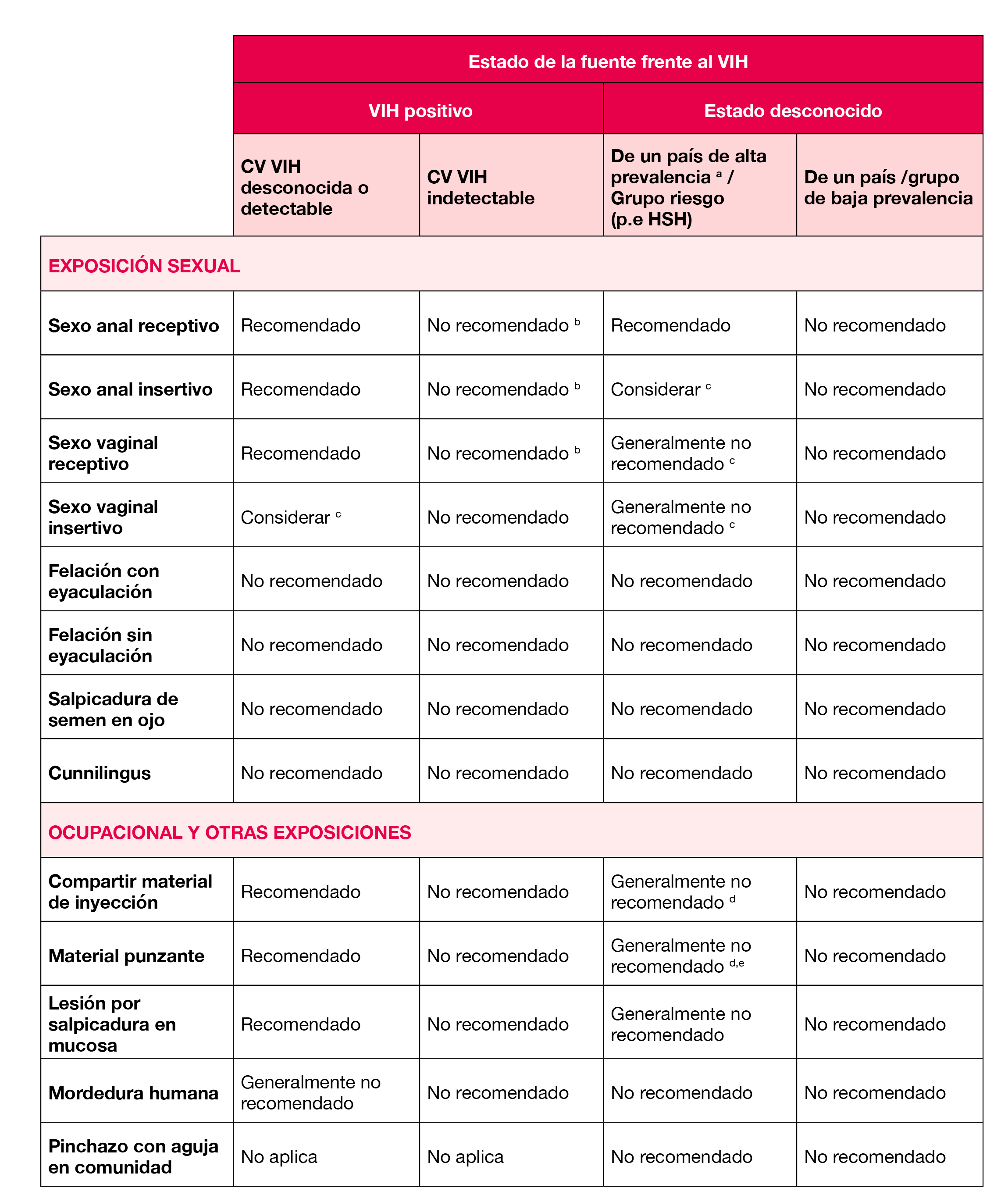
En la última edición de las Guías británicas de PPE 28, se ha publicado una estimación del riesgo de transmisión del VIH, según el tipo de exposición Tabla 1, y una estimación de la viremia en diferentes poblaciones de Gran Bretaña. Según estos datos y basándonos en la fórmula para el cálculo la probabilidad de transmisión de la infección
Riesgo de transmisión del VIH = riesgo de que la fuente sea VIH positiva con viremia detectable X riesgo inherente al tipo de exposición
podemos aproximarnos a una estimación más individualizada del riesgo de transmisión. Se considera de forma general, que en exposiciones con un riesgo inferior a 1 / 10 000, no se aconseja la administración de PPE. No obstante, la decisión debe ser individualizada y considerar posibles factores agravantes del riesgo de transmisión (relaciones traumáticas como es la agresión sexual, durante la menstruación o presencia de úlceras genitales o ITS concomitantes, …)
En la Tabla 2 se recogen las indicaciones para realizar PPE para el VIH tras exposición ocupacional y no ocupacional.
4.3.3. Evaluación del riesgo de transmisión no ocupacional del VHB y VHC
Dado que el VIH comparte vías de transmisión con el VHB y el VHC, en todas las situaciones comentadas previamente de riesgo para la ENO del VIH se deberá realizar la valoración de estas infecciones, así como su seguimiento serológico correspondiente.
En lo que respecta al VHB habrá que conocer el estado de la fuente y el estado de inmunidad del sujeto expuesto, y vacunar o utilizar gammaglobulina anti-VHB en caso necesario. En la Figura 1 se expone el algoritmo de actuación frente al VHB.
La transmisión del VHC por vía sexual ocurre primordialmente en HSH y, en un elevado porcentaje, con infección crónica por el VIH 3637 por tanto es importante valorar esta situación según las características de la relación y la persona fuente.
Evaluación de otras infecciones
(La mayoría aplican a las ENO por contacto sexual)
4.4.1. ITS
Tras una exposición sexual de riesgo, hay que tener en cuenta la posibilidad de transmisión de otras ITS, por ejemplo, sífilis, infección por Neisseria gonorrhoeae o por Chlamydia trachomatis , entre otras. Se ha reportado una prevalencia aproximada del 5 % de ITS, no detectadas en el cribado inicial basal, que se manifiestan en los 15 siguientes días a la exposición de riesgo. Por tanto, en aquellas personas que solicitan PPE se recomienda:
- Las personas asintomáticas deben ser evaluadas para ITS y la toma de muestras irá determinada por el tipo de práctica (sexo oral, vaginal, anal, insertivo / receptivo, etc.).
- Realizar una serología de sífilis.
- Realizar nueva valoración en el caso de experimentar algún síntoma sugestivo de ITS.
- Si hay síntomas de ITS presentes en el momento de la primera evaluación se requiere de una evaluación adicional, tratamiento empírico y seguimiento, de acuerdo con las guías nacionales de manejo del paciente con ITS.
4.4.2. Virus de la hepatitis A (VHA):
Es conveniente conocer el estado vacunal frente al VHA. En personas inmunocompetentes puede valorarse la indicación de una dosis de vacuna en las dos primeras semanas tras la exposición. La administración de inmunoglobulina como PPE frente al VHA puede ser de utilidad especialmente en personas inmunodeprimidas y ha de administrarse junto con una dosis de vacuna 38.
4.4.3. Mpox:
La vacunación puede ser utilizada como una forma de PPE en individuos sin síntomas que hayan tenido una exposición de riesgo a casos diagnosticados de mpox. Se debe realizar en los primeros 4 días tras el contacto (aunque podrá ofrecerse hasta los 14 días) 39.
4.4.3. Tétanos:
A las personas que sufran mordeduras, heridas o abrasiones se les debe evaluar su estado vacunal frente al tétanos y ofrecerles la profilaxis indicada 40.
Recomendaciones generales e indicación de PPE ante la exposición ocupacional y no ocupacional frente al VIH, VHB y VHC
- Tras una exposición cutánea debemos limpiar la zona con agua y jabón. Para las exposiciones percutáneas usar un antiséptico de base alcohólica ya que el alcohol tiene actividad viricida frente el VIH, VHB y VHC. En caso de una posible exposición sobre mucosas, se debe enjuagar la zona con abundante agua o irrigar con suero salino. Tras un pinchazo accidental, nunca debe exprimirse la zona del pinchazo. (AII)
- Se recomienda investigar la situación serológica frente al VIH de la persona fuente. (AI)
- En el caso de que la persona fuente tenga infección por el VIH conocida, es fundamental conocer la carga viral, el régimen de TAR (si lo recibe), así como la historia farmacológica y los motivos de cambio de tratamiento. (AI)
- Se recomienda PPE en exposiciones percutáneas con sangre si el riesgo es alto o muy alto. Si el riesgo es bajo, se evalúa la carga viral del paciente fuente, no siendo necesaria PPE si es indetectable. Para exposiciones de mucosas o piel de alto riesgo con sangre o líquidos infectantes, se recomienda PPE si la persona fuente presenta carga viral detectable. (AI)
- Si la PPE está indicada se recomienda iniciarla idealmente en las primeras 2 horas, preferiblemente en las primeras 12 horas, y siempre antes de las 72 horas. No se recomienda iniciar PPE si han pasado más de 72 horas desde la exposición. (AII)
- En el caso de la exposición ocupacional si no se puede conocer la situación serológica de la persona fuente, se valorarán las características clínicas y epidemiológicas y en caso de duda se considerará de alto riesgo. (BIII)
- En caso de una exposición no ocupacional sexual se debe valorar de forma individualizada la situación serológica de la fuente, y si esto no es posible, una estimación del riesgo teniendo en cuenta los datos epidemiológicos y el tipo de relación sexual. (BII)
- El sexo anal receptivo con eyaculación es la relación sexual asociada con un mayor riesgo de trasmisión del VIH, y es indicación para iniciar PPE si la persona fuente es VIH con carga viral detectable o desconocida o pertenece a un grupo de alta prevalencia de VIH (HSH o país de alta prevalencia). (AI)
- El sexo anal insertivo con persona fuente con VIH con carga viral detectable o desconocida es recomendación para iniciar PPE, y en el caso de persona fuente con estado serológico desconocido de un país o grupo de alta prevalencia se deberá considerar iniciar la PPE. (CII)
- El sexo vaginal receptivo con persona fuente con infección por VIH con carga viral detectable o desconocida es recomendación de iniciar PPE. Si se desconoce el estado serológico de la persona fuente, incluso si ésta pertenece a un grupo de alta prevalencia, generalmente no se recomienda PPE. (CII)
- En el sexo vaginal insertivo no se recomienda la PPE salvo sexo con persona con VIH con carga viral desconocida o detectable en el que se considerará. (CII)
- El sexo oral activo o pasivo no es indicación de PPE. (BII)
- Se recomienda individualizar, considerar la presencia de factores agravantes que incrementen el riesgo de transmisión del VIH, y valorar las preferencias de la persona expuesta respecto a la decisión de iniciar PPE. (CIII)
- Cuando se produce una exposición de riesgo, con independencia de si se realiza o no PPE, todos los procedimientos e intervenciones deben estar claramente recogidos en la historia clínica. (AI)
- En el caso del VHB la actuación depende de la situación tanto de la persona fuente como de la persona expuesta. (AII)
- Si la pauta de vacunación VHB es correcta, no debe efectuarse seguimiento salvo por las posibles implicaciones legales. (AII)
- En el caso de personas no vacunadas previamente o con vacunación incompleta, está indicada la profilaxis con IGHB y vacunación completa. (AII)
- En cuanto al VHC, no se dispone de PPE, las recomendaciones deben ir dirigidas a un diagnóstico y tratamiento precoz de una posible infección aguda. (AII)
Gráficos:
Tablas:


Bibliografía:
The path that ends AIDS: UNAIDS Global AIDS Update 2023. Geneva: Joint United Nations Programme on HIV/AIDS; 2023. Licence: CC BY-NC-SA 3.0 IGO. Accesible en:
https://thepath.unaids.org/wp-content/themes/unaids2023/assets/files/2023_report.pdf
Bourry O, Brochard P, Souquiere S, Maria Makuwa, Julien Calvo, Nathalie Dereudre-Bosquet, et al. Prevention of vaginal simian immunodeficiency virus transmission in macaques by postexposure prophylaxis with zidovudine, lamivudine and indinavir. AIDS. 2009; 23(4):447-54. doi: 10.1097/QAD.0b013e328321302d. PMID: 19240457.
Nielsen-Saines K, Watts DH, Veloso VG, Joao EC, Pilotto JH, Gray G, et al. Three postpartum antiretroviral regimens to prevent intrapartum HIV infection. N Engl J Med 2012; 366:2368-79. doi: 10.1056/NEJMoa1108275. PMID: 22716975; PMCID: PMC3590113.
Cardo DM, Culver DH, Ciesielski CA, P U Srivastava, R Marcus, D Abiteboul, et al. A case-control study of HIV seroconversion in health care workers after percutaneous exposure. Centers for Disease Control and Prevention Needlestick Surveillance Group. N Engl J Med. 1997; 337(21):1485-90. doi: 10.1056/NEJM199711203372101. PMID: 9366579.
Schechter M, do Lago RF, Mendelsohn AB, Ronaldo I Moreira, Lawrence H Moulton, Lee H Harrison et al. Behavioral impact, acceptability, and HIV incidence among homosexual men with access to postexposure chemoprophylaxis for HIV. J Acquir Immune Defic Syndr 2004; 35:519-25. doi: 10.1097/00126334-200404150-00010. PMID: 15021317.
Beymer MR, Weiss RE, Bolan RK, Kofron RM, Flynn RP, Pieribone DL et al. Differentiating Nonoccupational Postexposure Prophylaxis Seroconverters and Non-Seroconverters in a Community-Based Clinic in Los Angeles, California. Open Forum Infect Dis 2017 Apr 4;4(2):ofx061. doi: 10.1093/ofid/ofx061. eCollection 2017 Spring.
Kuhar DT, Henderson DK, Struble KA, Walid Heneine, Vasavi Thomas, Laura W Cheever, et al. Updated US Public Health Service guidelines for the management of occupational exposures to human immunodeficiency virus and recommendations for postexposure prophylaxis. Infect Control Hosp Epidemiol 2013 Sep;34(9):875-92. doi: 10.1086/672271. Erratum in: Infect Control Hosp Epidemiol. 2013 Nov;34(11):1238. Dosage error in article text. PMID: 23917901.
Cohen MS, Chen YQ, McCauley M, Gamble T, Hosseinipour MC, Kumarasamy N, et al. Prevention of HIV-1 infection with early antiretroviral therapy. N Engl J Med.2011; 365:493-505. doi: 10.1056/NEJMoa1105243. PMID: 21767103; PMCID: PMC3200068.
Masciotra S, McDougal JS, Feldman J, Patrick Sprinkle, Laura Wesolowski, S Michele Owen. Evaluation of an alternative HIV diagnostic algorithm using specimens from seroconversion panels and persons with established HIV infections. J Clin Virol 2011;52 Suppl 1: S17-22. doi: 10.1016/j.jcv.2011.09.011. PMID: 21981983.
Chávez P, Wesolowski L, Patel P, Anastos K, DeHovitz J, Kassaye SG, et al. Evaluation of the performance of the Abbott ARCHITECT HIV Ag/Ab Combo Assay. J Clin Virol 2011;52 Suppl 1:S 51-5. doi: 10.1016/j.jcv.2011.09.010. PMID: 21983253.
Documento de consenso de GeSIDA/ División de Control de VIH, ITS, Hepatitis virales y Tuberculosis del Ministerio de Sanidad respecto al tratamiento antirretroviral en adultos infectados por el virus de la inmunodeficiencia humana (Actualización enero 2023). Panel de expertos de GeSIDA y de la División de Control de VIH, ITS, Hepatitis virales y Tuberculosis del Ministerio de Sanidad. Accesible en:
https://gesida-seimc.org/wp-content/uploads/2023/06/Guia_TAR_V12.pdf
Centers for Disease Control and Prevention. Diagnoses of HIV infection in the United States and dependent areas, 2021. HIV Surveillance Report. 2021. Accesible en:
Furtado MR, Callaway DS, Phair JP, K J Kunstman, J L Stanton, C A Macken, et al. Persistence of HIV-1 transcription in peripheral-blood mononuclear cells in patients receiving potent antiretroviral therapy. N Engl J Med 1999; 340 (21):1614-22. doi: 10.1056/NEJM199905273402102. PMID: 10341273.
Ibáñez A, Puig T, Elías J, B Clotet, L Ruiz, M A Martínez. Quantification of integrated and total HIV-1 DNA after long-term highly active antiretroviral therapy in HIV-1-infected patients. AIDS 1999; 13 (9):1045-9. doi: 10.1097/00002030-199906180-00007. PMID: 10397534.
Bond WW, Favero MS, Petersen NJ, C R Gravelle, J W Ebert, J E Maynard. Survival of hepatitis B virus after drying and storage for one week. Lancet 1981 Mar 07;1(8219):550-1. doi: 10.1016/s0140-6736(81)92877-4. PMID: 6111645.
Werner BG, Grady GF. Accidental hepatitis B surface antigen positive innoculations: use of e antigen to estimate infectivity. Ann Intern Med 1982; 97: 367-9. doi: 10.7326/0003-4819-97-3-367. PMID: 7114632.
CDC Guidance for Evaluating Health-Care Personnel for Hepatitis B Virus Protection and for Administering Postexposure Management. MMWR Recomm Rep. 2013 Dec 20;62(RR-10):1-19. PMID: 24352112.
Unidad de vigilancia de VIH, ITS y hepatitis B y C. Indicadores clave: Hepatitis B y C. Centro Nacional de Epidemiología, Instituto de Salud Carlos III / División de Control de VIH, ITS, Hepatitis virales y Tuberculosis, Dirección General de Salud Pública; 2024. Accesible en:
Bruguera M. Hepatitis C esporádica: importancia relativa de la transmisión vertical, sexual y parenteral inaparente del virus de la hepatitis C. Med Clin (Barc) 1998 Nov 21;111(17):658-9. PMID: 9881348.
Serra C, Torres M, Campins M. Riesgo laboral de infección por el virus de la hepatitis C después de una exposición accidental. Grupo Catalán para el Estudio del Riesgo laboral de infección por el VHC en hospitales. Med Clin (Barc) 1998; Nov 21;111(17):645-9. PMID: 9881345.
Esteve M, Casas I, Planas R, Matas L. Hepatitis C aguda postinoculación accidental en un profesional sanitario con respuesta al tratamiento con interferón. Med Clin (Barc) 2000 Feb 5;114(4):157. doi: 10.1016/s0025-7753(00)71223-1. PMID: 10734627.
U.S. Public Health Service. Updated U.S. Public Health Service Guidelines for the Management of Occupational Exposures to HBV, HCV, and HIV and Recommendations for Postexposure Prophylaxis. MMWR Recomm Rep. 2001 Jun 29;50(RR-11):1-52. PMID: 11442229.
Moorman AC, de Perio MA, Goldschmidt R, Chu C, Kuhar D, Henderson DK, et al. Testing and Clinical Management of Health Care Personnel Potentially Exposed to Hepatitis C Virus - CDC Guidance, United States, 2020. MMWR Recomm Rep. 2020 Jul 24;69(6):1-8. doi: 10.15585/mmwr.rr6906a1. PMID: 32701942; PMCID: PMC8631757.
Rothenberg RB, Scarlett M, del Rio C, Reznik D, O'Daniels C, et al. Oral transmission of HIV. AIDS 1998; 12(16):2095-105. doi: 10.1097/00002030-199816000-00004. PMID: 9833850.
Rottingen JA, Cameron DW, Garnett GP. A systematic review of the epidemiologic interactions between classic sexually transmitted diseases and HIV: how much really is known? Sex Transm Dis 2001;28(10):579-97. doi: 10.1097/00007435-200110000-00005. PMID: 11689757.
Gray RH, Wawer MJ. Probability of heterosexual HIV-1 transmission per coital act in sub-Saharan Africa. The Journal of infectious diseases. 2012;205(3):351-2. doi: 10.1093/infdis/jir751. Epub 2012 Jan 11. PMID: 22241799.
Leynaert B, Downs AM, de Vincenzi I. Heterosexual transmission of human immunodeficiency virus: variability of infectivity throughout the course of infection. European Study Group on Heterosexual Transmission of HIV. American journal of epidemiology. 1998;148(1):88-96. doi: 10.1093/oxfordjournals.aje.a009564. PMID: 9663408.
Broyles LN, Luo R, Boeras D, Vojno L. The risk of sexual transmission of HIV in individuals with low-level HIV viraemia: a systematic review. Lancet 2023 Aug 5;402(10400):464-471. doi: 10.1016/S0140-6736(23)00877-2. Epub 2023 Jul 22. PMID: 37490935; PMCID: PMC10415671.
Cresswell F, Asanati K, Bhagani S, Boffito M, Delpech V, Ellis J, et al. UK guideline for the use of HIV post-exposure prophylaxis 2021. HIV Med. 2022 May;23(5):494-545. doi: 10.1111/hiv.13208. Erratum in: HIV Med. 2022 Jul;23(6):701. doi: 10.1111/hiv.13327. PMID: 35166004.
Wald A, Link K. Risk of human immunodeficiency virus infection in herpes simplex virus type 2-seropositive persons: a meta-analysis. J Infect Dis 2002;185(1):45-52. doi: 10.1086/338231. Epub 2001 Dec 14. PMID: 11756980.
Thomson KA, Hughes J, Baeten JM, Grace John-Stewart, Connie Celum, Craig R Cohen, et al. Increased Risk of HIV Acquisition Among Women Throughout Pregnancy and During the Postpartum Period: A Prospective Per-Coital-Act Analysis Among Women With HIV-Infected Partners. J Infect Dis 2018;218(1):16-25. doi: 10.1093/infdis/jiy113. PMID: 29514254; PMCID: PMC5989601.
Unidad de vigilancia de VIH, ITS y hepatitis B y C. Indicadores clave: Infección por VIH e Infecciones de Transmisión Sexual. Centro Nacional de Epidemiología, Instituto de Salud Carlos III / División de Control de VIH, ITS, Hepatitis virales y Tuberculosis, Dirección General de Salud Pública; 2024. Accesible en: https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/vigilancia/docs/INDICADORES_VIH_e_ITS_Febrero_2024.pdf
Unidad de vigilancia del VIH, ITS y hepatitis B y C. Actualización del Continuo de Atención del VIH en España, 2021. Madrid: Centro Nacional de Epidemiología – Instituto de Salud Carlos III/ División de control de VIH, ITS, Hepatitis Virales y Tuberculosis – Dirección General de Salud Pública; 2023. Accesible en: https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/vigilancia/docs/Continuo_atencion_VIH_mayo_2023.pdf
Encuesta sobre relaciones sociales y afectivas pospandemia III. Avance de resultados. Estudio nº 3040 . Centro de Investigaciones Sociológicas, Marzo de 2023. Accesible en: https://www.cis.es/documents/d/cis/es3400marmt_a
Encuesta europea on-line para hombres que tienen sexo con hombres (EMIS-2017): resultados en España. Ministerio de Sanidad, 2020. Accesible en: https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/docs/EMIS_Report_07052020.pdf
Observatorio Español de las Drogas y las Adicciones. Informe 2023. Alcohol, tabaco y drogas ilegales en España. Madrid: Ministerio de Sanidad. Delegación del Gobierno para el Plan Nacional sobre Drogas; 2023. Accesible en: https://pnsd.sanidad.gob.es/profesionales/sistemasInformacion/informesEstadisticas/pdf/2023OEDA-INFORME.pdf
Urbanus AT, van de Laar TJ, Stolte IG, Schinkel J, Heijman T, Coutinho RA, et al. Hepatitis C virus infections among HIV-infected men who have sex with men: an expanding epidemic. AIDS 2009; 23: F1-7. doi: 10.1097/QAD.0b013e32832e5631. PMID: 19542864.
Yaphe S, Bozinoff N, Kyle R, Shivkumar S, Pai NP, Klein M. Incidence of acute hepatitis C virus infection among men who have sex with men with and without HIV infection: a systematic review. Sex Transm Infect 2012; 88:558-64. doi: 10.1136/sextrans-2012-050566. PMID: 22859499.
Protocolo de vigilancia de la hepatitis A. Protocolos de la Red Nacional de Vigilancia Epidemiológica. Accesible en:
Recomendaciones de vacunación en el brote actual de viruela del mono. Ministerio de Sanidad. Comisión de Salud Pública de 9 de junio de 2022. Accesible en:
Grupo de trabajo recomendaciones Td 2017. Ponencia de Programa y Registro de Vacunaciones. Recomendaciones de utilización de vacunas Td. Comisión de Salud Pública del Consejo Interterritorial del Sistema Nacional de Salud. Ministerio de Sanidad, Servicios Sociales e Igualdad, 2017. Accesible en: https://www.sanidad.gob.es/areas/promocionPrevencion/vacunaciones/programasDeVacunacion/docs/TetanosDifteria_2017.pdf
5. PROFILAXIS POSEXPOSICIÓN EN SITUACIONES ESPECIALES
5.1. Pinchazo accidental en la comunidad
5.2. Agresiones sexuales
5.3. En personas gestantes y madres en periodo de lactancia
5.4. Tras mordedura humana
5.5. Particularidades de la PPE en contextos de PrEP
5.6. Particularidades de la PPE en usuarios de drogas inyectadas y chemsex
5.7. PPE para el VIH en personas en tratamiento crónico frente al VHB
Pinchazo accidental en la comunidad
PPE frente al VIH
En general, no se recomienda la PPE al VIH tras una exposición por pinchazo con aguja en la comunidad, ya que el riesgo es extremadamente bajo y normalmente no es posible determinar si se ha utilizado la aguja y con qué fin, el estado serológico respecto al VIH del caso índice y el intervalo entre el uso de la aguja y la exposición 1. (CII)
PPE frente a la hepatitis B
Si la fuente es HBsAg positiva: seguir indicaciones de la PPE ocupacional.
En caso de que la fuente sea HBsAg desconocida, si la persona expuesta tiene documentada la vacunación completa frente a la hepatitis B no precisa PPE. En caso de vacunación incompleta debe continuar la pauta pendiente. Si no tiene vacunación previa debe recibir pauta completa con la administración de la primera dosis en las primeras 24 h, y no más de 7 días después. Ver figura 4.1. 12. (AII)
PPE frente a la hepatitis C
No existen datos que respalden ninguna modalidad de PPE para prevenir la adquisición del VHC tras la exposición al virus. Existen tratamientos antivirales muy eficaces, y se recomienda un tratamiento precoz si se detecta seroconversión del VHC 13. (AII)
Agresiones sexuales
Dado que la presencia de abrasiones o lesiones en la mucosa vaginal o anal aumenta el riesgo de adquisición de VIH se cree que el riesgo sería mayor en personas supervivientes de agresión sexual, aunque no se ha publicado evidencia suficiente que lo apoye 4. Además, los datos sobre seroprevalencia de infección por VIH en agresores son poco conocidos y aún más su estado virológico. Se debe tratar como una exposición de alto riesgo.
Se recomienda PPE frente a VIH en situaciones de exposición significativa (BIII), la aplicación de protocolos médico-legales vigentes en el centro y la recomendación de tratamiento empírico de otras ITS. (AII)
No existen peculiaridades respecto a la profilaxis del VHB.
En personas gestantes y madres en periodo de lactancia
Los cambios biológicos durante el embarazo sugieren que las personas gestantes y en puerperio inmediato presentan un mayor riesgo de adquisición de VIH por vía sexual 5. Además, el riesgo de transmisión del VIH de madre a hijo durante el embarazo y la lactancia aumenta notablemente durante la infección aguda por VIH.
La indicación de profilaxis debe ser independiente del estado gestacional y estar guiada por la valoración de riesgo según el tipo de exposición. (CII)
En caso de estar indicada, la pauta preferente en una persona gestante será raltegravir 400 mg / 12 horas y emtricitabina 200 mg / tenofovir disoproxil 245 mg / 24 horas, durante 28 días (consultar tema 6, tabla 6.1.)Tabla 1. (AI)
La lactancia no es contraindicación para la PPE frente al VIH.
No existen diferencias respecto a la población general en cuanto a profilaxis frente al VHB.
Tras mordedura humana
Aunque existen algunos casos publicados de trasmisión tras mordeduras, la evidencia es escasa y de poca calidad 67.
En general, no se recomienda la PPE después de una mordedura ya que, aunque se desconoce el riesgo preciso de transmisión, es probable que sea insignificante. (BIII) Únicamente debería ofrecerse PPE si se cumplen 3 condiciones: carga viral VIH detectable (> 1000 copias/ml) en la fuente, saliva con abundante contenido de sangre y exposición con herida profunda. (CII)
Particularidades de la PPE en contextos de PrEP
Los usuarios de PrEP son un grupo que presenta alto riesgo de adquirir la infección VIH. En el caso de una potencial exposición reciente al VIH, se deberá plantear la PPE si la adherencia no es buena y la indicación dependerá del tiempo transcurrido desde la última dosis de PrEP y el tipo de exposición 89 Tabla 1 . (CIII)
Tras completar el tratamiento de 28 días de PPE y confirmarse la negatividad de la serología de VIH, habrá que valorar las posibles barreras o causas de la mala adherencia a la PrEP y reiniciarla si está indicada 9.
En los usuarios que solicitan la PrEP se debe evaluar la existencia de situaciones de riesgo en las 72 horas previas y en caso de indicación de PPE iniciarla, realizando la transición a la PrEP tras completar el tratamiento (BI) 9, sin necesidad de interrupción entre ambas, (BII), confirmando que no han adquirido la infección por VIH con una prueba serológica de 4a generación y/o CV de VIH (BI). Sin embargo, en caso de sospecha de infección aguda por VIH se debe continuar la PPE hasta descartarla completamente 9. (CIII)
Respecto a la profilaxis frente a la infección por VHB, existen datos de estudios que muestran una protección del tratamiento con TDF/FTC frente a la infección VHB 10, no obstante, las recomendaciones actuales son las mismas que para el resto de personas.
Particularidades de la PPE en usuarios de drogas inyectadas y chemsex
La infección por el VIH y las hepatitis B y C se pueden transmitir en personas que usan drogas por vía parenteral mediante el intercambio de jeringuillas y otros materiales de inyección con sangre contaminada. Esto incluye el uso sexualizado de drogas administradas por vía intravenosa (slamming o slamsex). En HSH se debe preguntar específicamente por el uso de drogas, chemsex y slamsex 1. Algunos estudios reflejan un retraso en el inicio de la PPE en este contexto, dado que el consumo de drogas unido a sesiones de sexo de larga duración, pueden llevar a una menor percepción del riesgo o hacerlo de forma diferida. Es posible que algunas personas consulten por otros problemas derivados del consumo de dichas drogas, siendo esta una oportunidad para evaluar los contactos de riesgo recientes y ofrecer la PPE cuando esté indicada 11, (BIII). En los casos de slamsex es difícil separar el riesgo de transmisión del VIH a través de la vía intravenosa o de la vía sexual, por lo que habrá que considerar ambas exposiciones en la evaluación del riesgo. (CII)
El riesgo y fundamentos de la transmisión percutánea no ocupacional para VIH, VHB y VHC son similares a los de la transmisión ocupacional, excepto por la frecuente dificultad para identificar la fuente de exposición que caracteriza a la exposición no ocupacional 12.
Según estimaciones, el riesgo de transmisión del VIH por cada exposición a través de agujas compartidas es aproximadamente del 0,7 % (1 de cada 149 exposiciones) (Tema 4, tabla 4.1.). Este riesgo puede variar según factores como la carga viral del individuo infectado y la frecuencia del intercambio de agujas. Por este motivo, se recomienda la PPE tras haber compartido material de inyección si la fuente es una persona con VIH positivo sin TAR, con mal cumplimiento del mismo o CV detectable 13. (CI)
PPE para el VIH en personas en tratamiento crónico frente al VHB
Se ha objetivado que el TDF en monoterapia puede ser eficaz como profilaxis preexposición para VIH en varones heterosexuales y mujeres y, posiblemente, para varones HSH. No obstante, se han descrito infecciones de brecha y, por lo tanto, en estas personas se debe considerar realizar la PPE con las pautas recomendadas de triple terapia 14, salvo en los casos en los que la persona expuesta estuviese en tratamiento bajo terapia combinada (TDF/FTC, TAF/FTC) y se confirmara una buena adherencia a la misma. (AII)
En base a los datos que conocemos de la PrEP el riesgo de alteraciones hepáticas tras su suspensión en pacientes sin cirrosis es bajo 15, suspender la PPE sería relativamente seguro en pacientes con hepatitis B crónica sin tratamiento ni indicación del mismo previamente, aunque es aconsejable valorar la situación junto con un especialista en hepatitis virales (BII). No se considera que exista riesgo de que el VHB desarrolle resistencia frente a tenofovir o emtricitabina/lamivudina tras 28 días de terapia combinada.
En los casos en que se diagnostique infección activa por VHB en la evaluación inicial, no se debe retrasar el inicio de la PPE según esté indicada, y se deberá mantener hasta consultar con un especialista en hepatitis virales para valorar su suspensión tras finalizar la PPE. (BI)
Tablas:

Considerar INICIAR PPE frente a VIH en pacientes en PrEP si:
Bibliografía:
Cresswell F, Asanati K, Bhagani S, Boffito M, Delpech V, Ellis J, et al. UK guideline for the use of HIV post-exposure prophylaxis 2021. HIV Med. 2022 May;23(5):494-545. doi: 10.1111/hiv.13208. Epub 2022 Feb 14. Erratum in: HIV Med. 2022 Jul;23(6):701. doi: 10.1111/hiv.13327. PMID: 35166004.
Schillie S, Vellozzi C, Reingold A, Harris A, Haber P, Ward JW, et al. Prevention of Hepatitis B Virus Infection in the United States: Recommendations of the Advisory Committee on Immunization Practices. MMWR Recomm Rep 2018;67(No. RR-1):1–31. DOI: http://dx.doi.org/10.15585/mmwr.rr6701a1. PMID: 29939980; PMCID: PMC5837403.
Moorman AC, de Perio MA, Goldschmidt R, Chu C, Kuhar D, Henderson DK, et al. Testing and clinical management of health care personnel potentially exposed to hepatitis C virus. CDC Guidance, United States, 2020. MMWR Recomm Rep 2020;69:1-8. PMID: 32701942; PMCID: PMC8631757.
Scannell-Tocci M, Reynolds R. A review of sexual transmitted infection rates among sexually assaulted patients that present for care. Journal of Forensic and Legal Medicine 2022; 88:102352. doi:10.1016/j.jflm.2022.102352. PMID: 35512505.
Thomson KA, Hughes J, Baeten JM, John-Stewart G, Celum C, Cohen CR, et al. Increased Risk of HIV Acquisition Among Women Throughout Pregnancy and During the Postpartum Period: A Prospective Per-Coital-Act Analysis Among Women With HIV-Infected Partners. J Infect Dis. 2018 Jun 5;218(1):16-25. doi: 10.1093/infdis/jiy113. PMID: 29514254; PMCID: PMC5989601.
Cresswell FV, Ellis J, Hartley J, Sabin CA, Orkin C, Churchill DR. A systematic review of risk of HIV transmission through biting or spitting: implications for policy. HIV Med. 2018 Apr 23;19(8):532–40. doi: 10.1111/hiv.12625. PMID: 29687590; PMCID: PMC6120498.
Thomas MG, Hopkins CJ, Luey CE. Transmission of HIV infection by severe bites. Int J STD AIDS. 2019 Aug;30(9):927-929. doi: 10.1177/0956462419844852. PMID: 31226915.
EACS guidelines version 12.1. European AIDS Clinical Society; 2024. https://www.eacsociety.org/guidelines/eacs-guidelines/
US Public Health Service: Preexposure prophylaxis for the prevention of HIV in the United States - 2021 update, a clinical practice guideline. https://stacks.cdc.gov/view/cdc/112360
Mizushima D, Takano M, Aoki T, Ando N, Uemura H, Yanagawa Y, et al. Effect of tenofovir-based HIV pre-exposure prophylaxis against HBV infection in men who have sex with men. Hepatology. 2023 Jun 1;77(6):2084-2092. doi: 10.1097/HEP.0000000000000384. PMID: 36960800; PMCID: PMC10187616.
Casalino E, Bouzid D, Antoniol S, Pinto A, Choquet C, Pereira L, et al. Characteristics of human immunodeficiency virus exposure and predictors of time until access to postexposure prophylaxis: a prospective observational study. Emergencias. 2021 Feb;33(1):35-41. English, Spanish. PMID: 33496398.
Documento de Consenso sobre profilaxis postexposición ocupacional y no ocupacional en relación con el VIH, VHB y VHC en adultos y niños. (Actualización 2015). Guías GESIDA. https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/hepatitisC/informacion/docs/Profilaxis_postexposicion_ocupacional_y_no_ocupacional_VIH_VHB_VHC(PPE).pdf
Updated Guidelines for Antiretroviral Postexposure Prophylaxis After Sexual, Injection Drug Use, or Other Nonoccupational Exposure to HIV—United States, 2016 from the Centers for Disease Control and Prevention, U.S. Department of Health and Human Services. Accesible en: https://stacks.cdc.gov/view/cdc/38856
Fox J, Brady M, Alexander H, Davies O, Robinson N, Pace M, et al. Tenofovir Disoproxil Fumarate Fails to Prevent HIV Acquisition or the Establishment of a Viral Reservoir: Two Case Reports. Infect Dis Ther. 2016 Mar;5(1):65-71. doi: 10.1007/s40121-015-0102-x. PMID: 26746652; PMCID: PMC4811833.
Solomon MM, Schechter M, Liu AY, McMahan VM, Guanira JV, Hance RJ, et al. The Safety of Tenofovir-Emtricitabine for HIV Pre-Exposure Prophylaxis (PrEP) in Individuals With Active Hepatitis B. J Acquir Immune Defic Syndr. 2016 Mar 1;71(3):281-6. doi: 10.1097/QAI.0000000000000857. Erratum in: J Acquir Immune Defic Syndr. 2016 Jul 1;72(3):e82. doi: 10.1097/QAI.0000000000001100. PMID: 26413853; PMCID: PMC4752387.
6. PAUTAS DE PROFILAXIS POSEXPOSICIÓN
6.1. Eficacia y elección de tratamiento
6.2. Inicio y duración de PPE
6.3. Toxicidad
6.4. Interacciones
6.5. Recomendaciones
Eficacia y elección de tratamiento
Aunque no es posible establecer recomendaciones estrictamente basadas en la eficacia, es crucial considerar la evidencia científica disponible, la experiencia, la tolerabilidad y los beneficios asociados a la pauta de dosificación y la existencia o no de interacciones. A pesar de que hay unas pautas generales recomendadas, las características de la persona fuente o las comorbilidades de la persona expuesta pueden determinar la elección de pautas distintas. Hay que tener en cuenta que el TDF puede producir toxicidad renal y que está contraindicado en pacientes con insuficiencia renal.
Las opciones de tratamiento se han seleccionado basándose en los datos de eficacia, seguridad, tolerabilidad y disponibilidad, además de experiencia clínica.
6.1.1. Pautas de elección:
- Raltegravir más tenofovir disoproxil fumarato / emtricitabina (RAL + TDF/FTC): esta combinación es ampliamente recomendada por su experiencia de uso 1, es una pauta bien tolerada y tiene mínimas interacciones farmacológicas, (AI). El principal inconveniente es su posología cada 12 horas, aunque existe recomendación para una dosis diaria 2. (AIII)
- Dolutegravir más tenofovir disoproxil fumarato / emtricitabina (DTG + TDF/FTC): es una pauta bien tolerada y tiene mínimas interacciones farmacológicas 3. Se administran los dos comprimidos de forma conjunta una vez al día. (AII)
- Doravirina / lamivudina / tenofovir disoproxil fumarato o Doravirina más tenofovir-disoproxil / emtricitabina (DOR/3TC/TDF o DOR + TDF/FTC): es un tratamiento bien tolerado que ha demostrado bajas tasas de discontinuación (2 %) 4 (AII). No disponemos en España de la combinación DOR/3TC/TDF en un comprimido.
- Bictegravir / tenofovir alafenamida / emtricitabina (BIC/TAF/FTC): existen datos de buena tolerabilidad y pocas discontinuaciones para PPE en dos pequeñas cohortes retrospectivas 6 y recomendaciones recientes como pauta preferente 8. (AII)
6.1.2 Pautas alternativas:
- Rilpivirina / tenofovir disoproxil fumarato / emtricitabina (RPV/TDF/FTC): es una combinación bien tolerada y su uso está respaldado por experiencias comunicadas en distintos países, además de estudios prospectivos en cohortes multicéntricas 9. (BI)
- Darunavir más ritonavir más tenofovir disoproxil / emtricitabina (DRV + RTV + TDF/FTC): tiene una alta barrera genética a la resistencia y es mejor tolerado que otras opciones de IPs. Hay que tener en cuenta las interacciones farmacológicas y la posología de administración cada 12 horas, sería una pauta alternativa en personas gestantes cuando hay intolerancia a RAL o DTG. (BI)
- Darunavir / cobicistat/ tenofovir alafenamida / emtricitabina (DRV/c/TAF/FTC): Las ventajas respecto a DRV + RTV + TDF/FTC son la coformulación en un comprimido único y el uso de TAF en lugar de TDF. (BIII)
Inicio y duración de PPE
Se aconseja iniciar el tratamiento, idealmente en las primeras 2 horas, preferiblemente en las primeras 12 horas, y siempre antes de las 72 horas tras la exposición y con una duración de 28 días (AIII). Aunque hay estudios que sugieren que la eficacia es máxima con una sola dosis de fármaco las primeras 2 horas en modelos animales 11, no se disponen de datos que justifiquen recomendar pautas más cortas debido a la falta de evidencia sobre su eficacia. (AIII)
La terapia con 3 fármacos es la terapia habitual recomendada debido a la mayor probabilidad de una mayor eficacia; los regímenes actuales recomendados tienen una excelente tolerabilidad, sin embargo, si esto fuese una preocupación, el uso de un régimen de 2 fármacos sería preferible a suspender el régimen por completo 8.
Toxicidad
La combinación TDF/FTC como terapia principal es más tolerable y provoca menos abandonos por efectos secundarios que la terapia ZDV/3TC 12.
Los inhibidores de la transcriptasa inversa no análogos de nucleósidos como RPV combinado con TDF/FTC (TDF/FTC/RPV) mostraron en HSH unas tasas altas de tolerabilidad y adherencia. Aunque el 70 % experimentó efectos adversos relacionados con RPV, sólo el 3 % discontinuó la PPE. La combinación DOR/3TC/TDF mostró efectos adversos leves, con sólo un 2 % de discontinuaciones 4.
Los inhibidores de integrasa para la PPE, como en la combinación TDF/FTC y DTG, presentan buena tolerabilidad, con astenia, náuseas, diarrea y cefalea como efectos más habituales 3. En cuanto a RAL, en combinación con TDF/FTC, los efectos adversos observados son similares al resto de inhibidores de integrasa, y estos efectos son comparativamente menores a los observados con pautas que incluyen IP, donde los eventos adversos gastrointestinales como náuseas, diarrea y vómitos son más frecuentes y las tasas de discontinuación hasta del 10 % - 18 % . En caso de efectos adversos graves con una PPE previa, se debe optar por otro tratamiento disponible.
Interacciones
Se debe verificar el historial de medicación de la persona expuesta, incluidos medicamentos sin receta, vitaminas, productos de herboristería y drogas recreativas, antes de prescribir PPE para evitar interacciones medicamentosas significativas.
Los inhibidores de integrasa RAL, DTG y BIC, se unen a cationes como hierro y magnesio, reduciendo la absorción y los niveles del fármaco en sangre. Es preferible evitar antiácidos y suplementos con estos cationes o separar su ingesta de los inhibidores de integrasa al menos 4 horas, o bien cambiar a antiácidos sin cationes y suspender suplementos minerales como sales de hierro o multivitamínicos.
En el caso de fármacos con potenciadores metabólicos (ritonavir o cobicistat) hay que evitar estatinas, ergotamínicos, psicotrópicos, corticoides y anticonvulsivantes. En las mujeres en edad fértil que toman anticonceptivos no se recomienda esta pauta por las posibles interacciones. La rifampicina puede reducir las concentraciones de fármacos, por lo que, si fuera necesario,se aconseja el uso de RAL o DTG a doble dosis.
Es importante verificar posibles interacciones medicamentosas. (Universidad de Liverpool https://www.hiv-druginteractions.org/checker, Medscape https://reference.medscape.com/drug-interactionchecker).
Recomendaciones
- Se aconseja iniciar la PPE, idealmente en las primeras 2 horas, preferiblemente en las primeras 12 horas, y siempre antes de las 72 horas. (AII)
- La duración de la PPE debe ser de 28 días. (AII)
- Las pautas preferentes están basadas en TDF/FTC (salvo en pacientes con insuficiencia renal) (AI) y un tercer fármaco, de elección RAL o DTG (AI-AII) o DOR (AII), o bien la pauta de BIC/TAF/FTC. (AII).
- Las pautas alternativas están basadas en RPV/TDF/FTC/ (BI) y DRV/C/TAF/FTC. (BIII)
- La elección del tratamiento depende de las características de la persona fuente y las de la persona expuesta. (AII)
- Hay que revisar las interacciones antes de la prescripción de la PPE. (AII)
Tablas:
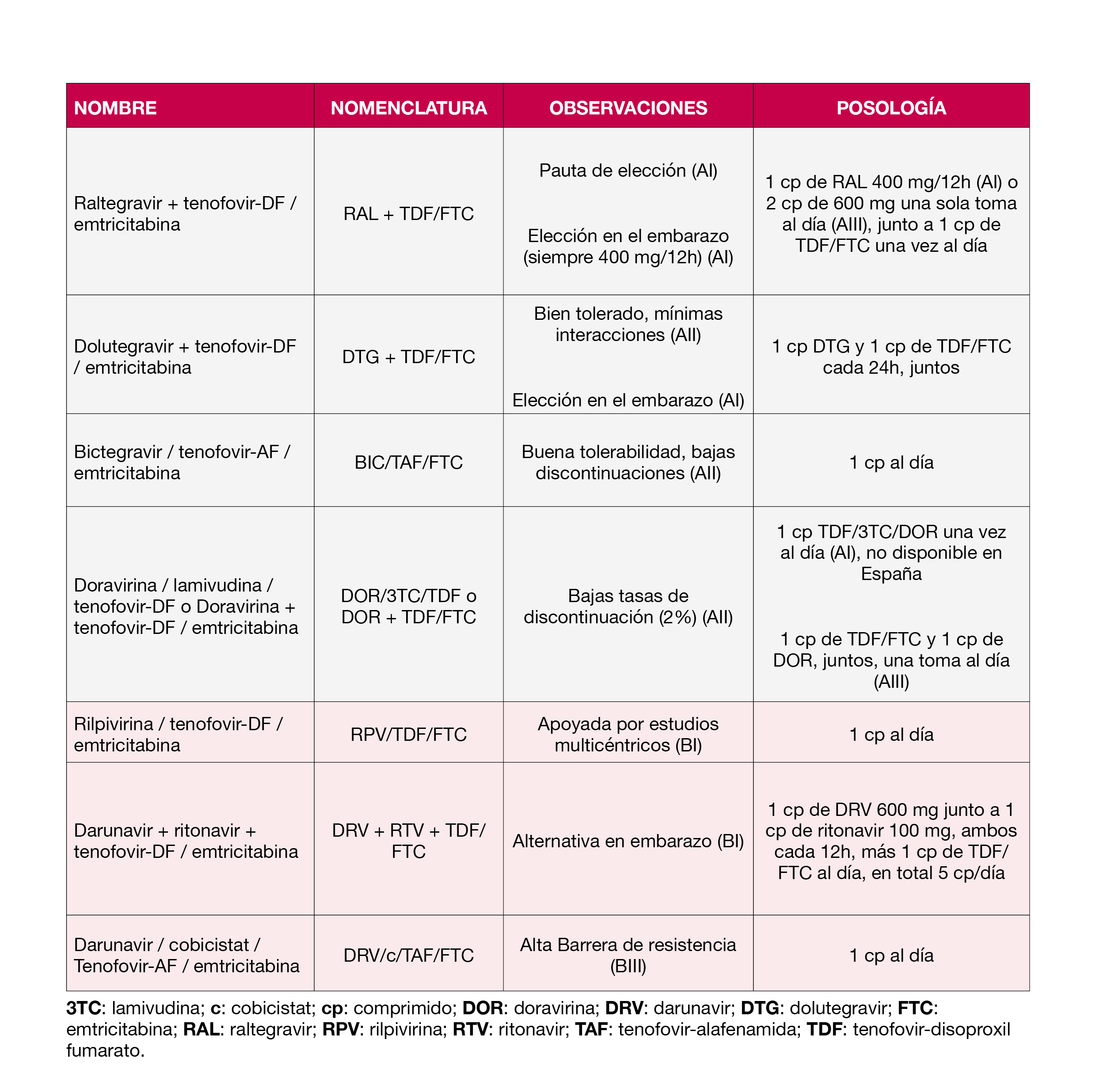
Bibliografía:
Leal L, León A, Torres B, Inciarte A, Lucero C, Mallolas J, Laguno M, el al. A randomized clinical trial comparing ritonavir-boosted lopinavir versus raltegravir each with tenofovir plus emtricitabine for post-exposure prophylaxis for HIV infection. J Antimicrob Chemother. 2016 Jul;71(7):1987-93. doi: 10.1093/jac/dkw049. PMID: 26994089 .
Quah SP, McIntyre M, Wood A, Mc Mullan K, Rafferty P. Once-daily raltegravir with tenofovir disoproxil/emtricitabine as HIV post-exposure prophylaxis following sexual exposure. HIV Med. 2021 Feb;22(2):e5-e6. doi: 10.1111/hiv.12938. PMID: 33063431.
McAllister JW, Towns JM, Mcnulty A, Pierce AB, Foster R, Richardson R, et al. Dolutegravir with tenofovir disoproxil fumarate-emtricitabine as HIV postexposure prophylaxis in gay and bisexual men. AIDS. 2017 Jun 1;31(9):1291-1295. doi: 10.1097/QAD.0000000000001447. PMID: 28301425.
Inciarte A, Ugarte A, Martínez-Rebollar M, Torres B, Fernández E, Berrocal L, et al. Doravirine/Lamivudine/Tenofovir Disoproxil Fumarate for Nonoccupational HIV-1 Postexposure Prophylaxis: A Prospective Open-Label Trial (DORAVIPEP). Open Forum Infect Dis. 2023 Jul 19;10(8):ofad374. doi: 10.1093/ofid/ofad374. PMID: 37539061; PMCID: PMC10394723.
Devred I, Kayembe K, Valin N, Rougier H, Shinga BW, Lambert-Niclot S, Chiarabini T, Meyohas MC, Lacombe K. Prophylaxis by doravirine-lamivudine- tenofovir disoproxil fumarate or elvitegravir-cobicistat-emtricitabine- tenofovir alafenamide after sexual exposure to HIV. BMC Infect Dis. 2023 Sep 4;23(1):578. doi: 10.1186/s12879-023-08544-x. PMID: 37667182; PMCID: PMC10478445.
Liu A, Xin R, Zhang H, Dai L, Wu RE, Wang X, et al. An open-label evaluation of safety and tolerability of coformulated bictegravir/emtricitabine/tenofovir alafenamide for post-exposure prophylaxis following potential exposure to human immunodeficiency virus-1. Chin Med J (Engl). 2022 Nov 20;135(22):2725-2729. doi: 10.1097/CM9.0000000000002494. PMID: 36719359; PMCID: PMC9944392.
Mayer KH, Gelman M, Holmes J, Kraft J, Melbourne K, Mimiaga MJ. Safety and Tolerability of Once Daily Coformulated Bictegravir, Emtricitabine, and Tenofovir Alafenamide for Postexposure Prophylaxis After Sexual Exposure. J Acquir Immune Defic Syndr. 2022 May 1;90(1):27-32. doi: 10.1097/QAI.0000000000002912. PMID: 34991141.
New York State Department of Health and AIDS Institute Guideline. Post-Exposure Prophylaxis (PEP) to Prevent HIV Infection. Actualización 3 de octubre de 2024. Accesible en: https://www.hivguidelines.org/guideline/hiv-pep/?mycollection=pep-prep
Chauveau M, Billaud E, Bonnet B, Merrien D, Hitoto H, Bouchez S, et al. Tenofovir DF/emtricitabine/rilpivirine as HIV post-exposure prophylaxis: results from a multicentre prospective study. J Antimicrob Chemother. 2019 Apr 1;74(4):1021-1027. doi: 10.1093/jac/dky547. PMID: 30689937.
Foster R, McAllister J, Read TR, Pierce AB, Richardson R, McNulty A, et al. Single-Tablet Emtricitabine-Rilpivirine-Tenofovir as HIV Postexposure Prophylaxis in Men Who Have Sex With Men. Clin Infect Dis. 2015 Oct 15;61(8):1336-41. doi: 10.1093/cid/civ511. PMID: 26123937.
Massud I, Ruone S, Zlotorzynska M, Haaland R, Mills P, Cong ME, et al. Single oral dose for HIV pre or post-exposure prophylaxis: user desirability and biological efficacy in macaques. EBioMedicine. 2020 Aug;58:102894. doi: 10.1016/j.ebiom.2020.102894. Epub 2020 Jul 21. Erratum in: EBioMedicine. 2024 Mar;101:105014. doi: 10.1016/j.ebiom.2024.105014. PMID: 32707451; PMCID: PMC7381488.
Ford N, Shubber Z, Calmy A, Irvine C, Rapparini C, Ajose O, et al. Choice of antiretroviral drugs for postexposure prophylaxis for adults and adolescents: a systematic review. Clin Infect Dis. 2015 Jun 1;60 Suppl 3:S170-6. doi: 10.1093/cid/civ092. PMID: 25972499.
Thomas R, Galanakis C, Vézina S, Longpré D, Boissonnault M, Huchet E, et al. Adherence to Post-Exposure Prophylaxis (PEP) and Incidence of HIV Seroconversion in a Major North American Cohort. PLoS One. 2015 Nov 11;10(11):e0142534. doi: 10.1371/journal.pone.0142534. PMID: 26559816; PMCID: PMC4641668.
Fätkenheuer G, Jessen H, Stoehr A, Jung N, Jessen AB, Kümmerle T, et al. PEPDar: A randomized prospective noninferiority study of ritonavir-boosted darunavir for HIV post-exposure prophylaxis. HIV Med. 2016 Jun;17(6):453-9. doi: 10.1111/hiv.12363. PMID: 27166295.
Milinkovic A, Benn P, Arenas-Pinto A, Brima N, Copas A, Clarke A, et al. Randomized controlled trial of the tolerability and completion of maraviroc compared with Kaletra® in combination with Truvada® for HIV post-exposure prophylaxis (MiPEP Trial). J Antimicrob Chemother. 2017 Jun 1;72(6):1760-1768. doi: 10.1093/jac/dkx062. PMID: 28369381.
Inciarte A, Leal L, González E, León A, Lucero C, Mallolas J, et al. Tenofovir disoproxil fumarate/emtricitabine plus ritonavir-boosted lopinavir or cobicistat-boosted elvitegravir as a single-tablet regimen for HIV post-exposure prophylaxis. J Antimicrob Chemother. 2017 Oct 1;72(10):2857-2861. doi: 10.1093/jac/dkx246. PMID: 29091217.
Fernández I, de Lazzari E, Inciarte A, Díaz-Brito V, Milinkovic A, Arenas-Pinto A, et al. Network meta-analysis of post-exposure prophylaxis randomized clinical trials. HIV Med. 2021 Mar;22(3):218-224. doi: 10.1111/hiv.12964. PMID: 33108035.
7. SEGUIMIENTO
A toda persona que haya sido evaluada tras una exposición ocupacional o no ocupacional, con independencia de que se realice PPE o no, se le debe ofrecer un plan de seguimiento clínico y analítico, información y apoyo psicológico. En caso de agresión sexual se debe ofrecer apoyo psicológico y social, y en el caso concreto de una mujer se debería realizar valoración por ginecología.
Analítica basal
Ha de realizarse lo antes posible, siempre en las primeras 72 horas tras la exposición.
Caso fuente (si es posible):
- Test combinado Anti-VIH 1-2 y Ag-p24 (4ª generación)
Si es positivo, completar proceso diagnóstico habitual (no urgente): carga viral y estudio de resistencias
- Ac VHC
Si es positivo, completar proceso diagnóstico habitual (no urgente) para detección de infección activa (ARN VHC o Ag VHC)
- HBsAg
Si es positivo, completar el perfil serológico y realizar determinación de carga viral plasmática (ADN VHB; no urgente). Realizar serología de VHD.
Si la persona fuente no da el consentimiento para la realización de las determinaciones serológicas, es desconocido o no puede realizarse, debe considerarse la fuente como de potencial riesgo.
Persona expuesta:
- Test combinado Anti-VIH 1/2 y Ag-p24 (4ª generación)
- Anti-VHC
- Anti-HBs (realizar si susceptible[1] y en inmunodeprimidos)
Añadir prueba de Anti-HBc y HBsAg en caso de Anti-HBs < 10 UI/ml
- Analítica que incluya bioquímica (perfil renal y hepático)
- En exposición sexual es necesario descartar otras ITS
- En mujeres en edad fértil, test de embarazo
Seguimiento
Las unidades de VIH o servicios especializados en VIH, los servicios de Salud Laboral y de Medicina Preventiva y Salud Pública, realizan el seguimiento de estos pacientes.
Es muy importante instruir al paciente sobre los síntomas de infección aguda por VIH, VHB y/o VHC para que consulte urgentemente si los presenta.
Toda persona expuesta se beneficiará de una evaluación inicial. Independientemente de la toma o no de la PPE, se recomienda al menos una evaluación de seguimiento. El momento de su realización dependerá del tipo de exposición y sobre todo de la posibilidad de encadenar profilaxis preexposición tras completar la pauta de PPE.
[1] Se considera susceptible cuando la persona no está vacunada o presenta un título de anti-HBs < 10 mUI/ml y es Anti-HBc negativo. La protección vacunal es superior al 90 % hasta 30 años después de la pauta inicial.
VIH
La evaluación clínica incluirá la valoración de la tolerancia y adherencia a la pauta de PPE.
Se suspenderá la PPE si la fuente ha resultado negativa o indetectable para VIH.
Al finalizar el periodo de 28 días de PPE se realizará nuevo test de VIH, bioquímica con perfil renal y hepático y, en mujeres en edad fértil, test de embarazo. Es importante valorar la necesidad de PrEP antes de finalizar la PPE para facilitar la continuidad de la prevención.
Si disponemos de un test combinado de VIH de 4a generación (Anti-VIH 1/2 y Ag-p24), el seguimiento finalizará a las 12 semanas posexposición. En los casos en los que no existen riesgo de transmisión de hepatitis y que no han llegado a tomar la PPE un test de 4ª generación en la semana 6 permite descartar la infección por VIH 5.
En caso de que la serología de VIH resulte positiva:
- Realizar determinación de carga viral plasmática de VIH urgente con estudio de resistencias
- No debe interrumpirse la PPE hasta que se confirme la primoinfección y se optimice el tratamiento antirretroviral.
VHB
Si anti-HBs ≥ 10 UI/ml, se considera inmune y no sería necesario realizar seguimiento (independientemente del resultado del HBsAg de la fuente).
Si se ha administrado una dosis de recuerdo de vacuna de VHB, se solicitarán anti-HBs para evaluar la respuesta (en 4-8 semanas).
Si la fuente es HBsAg + o de un grupo de alta prevalencia y la persona expuesta no inmune, se recomiendan controles adicionales para descartar la infección aguda por VHB (valorar hasta 24 semanas).
En caso que la determinación de HBsAg resulte positiva:
- Completar el perfil serológico (IgM anti-HBc, IgG anti-HBc, HBe Ag, anti-HBe)
- Realizar determinación de carga viral plasmática del VHB (ADN VHB)
- Realizar diagnóstico reflejo de VHD
- Valorar la necesidad de iniciar tratamiento frente al VHB
VHC
Se recomienda realizar una prueba de anticuerpos anti-VHC en la visita final de seguimiento tras la exposición.
Si la exposición es de alto riesgo (ejemplo, persona fuente VHC positivo) es preferible realizar ARN VHC o Ag VHC a las dos semanas de la exposición; el seguimiento se extendería en este caso hasta las 24 semanas posexposición.
En caso de que la prueba de anticuerpos anti-VHC resulte positiva:
- Realizar determinación de la carga viral plasmática del VHC (ARN VHC).
- Todas las personas infectadas deberían recibir tratamiento con AAD para erradicar el VHC, independientemente del estado de fibrosis hepática.
ITS
Es necesario realizar nuevo test de sífilis a las 12 semanas posexposición o en la última visita de seguimiento.
Se debe valorar la profilaxis posexposición de ITS con doxiciclina según las recomendaciones vigentes 6.
Se puede repetir el cribado de ITS a las dos semanas de la exposición en personas que presenten síntomas o a criterio del clínico responsable.
RECOMENDACIONES:
- Es necesario evaluar la adherencia y tolerancia a la PPE durante las 4 semanas de tratamiento. Se suspenderá la PPE si la fuente ha resultado negativa o la CV plasmática de VIH es indetectable. (AI)
- En individuos expuestos con anti-HBs ≥ 10 mIU/ml no es necesario realizar seguimiento de la infección por VHB, salvo por razones legales. (AIII)
- Se debe informar a los casos expuestos sobre medidas de prevención (uso de anticonceptivos de barrera, evitar las donaciones de sangre o derivados, tejidos o semen, el embarazo o la lactancia) para prevenir la transmisión secundaria.(AII)
Tablas:
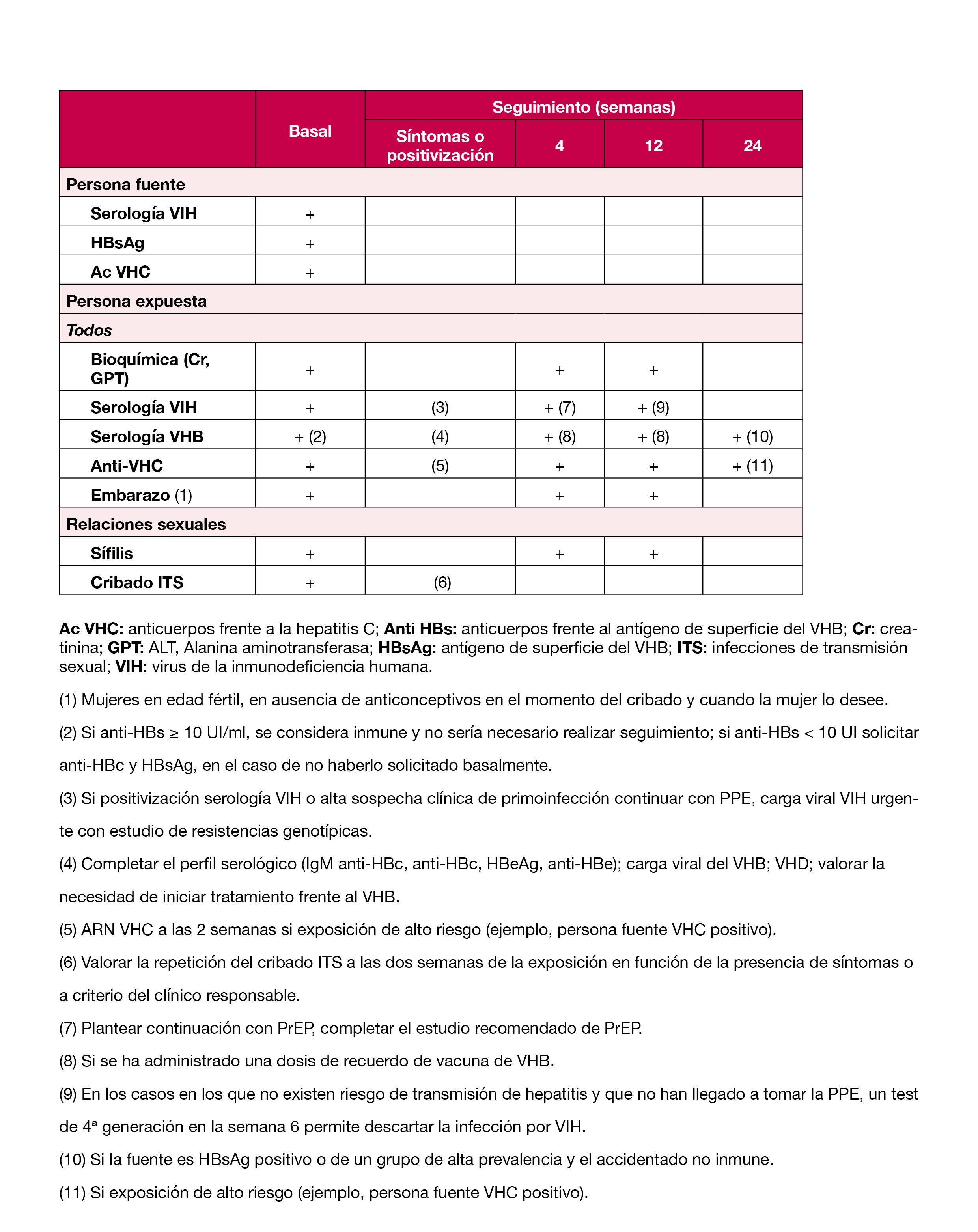
Bibliografía:
Inciarte A, Leal L, Masfarre L, González E, Díaz-Brito V, Lucero C, et al; Sexual Assault Victims Study Group. Post-exposure prophylaxis for HIV infection in sexual assault victims. HIV Med. 2020 Jan;21(1):43-52. doi: 10.1111/hiv.12797. PMID: 31603619; PMCID: PMC6916272.
DeHaan E, McGowan JP, Fine SM, et al. PEP to Prevent HIV Infection [Internet]. Baltimore (MD): Johns Hopkins University; 2022 Aug 11. Available from: https://www.ncbi.nlm.nih.gov/books/NBK562734/
Schillie S, Vellozzi C, Reingold A, Harris A, Haber P, Ward JW, et al. Prevention of Hepatitis B Virus Infection in the United States: Recommendations of the Advisory Committee on Immunization Practices. MMWR Recomm Rep. 2018 Jan 12;67(1):1-31. doi: 10.15585/mmwr.rr6701a1. PMID: 29939980; PMCID: PMC5837403.
Bruce MG, Bruden D, Hurlburt D, Zanis C, Thompson G, Rea L, et al. Antibody Levels and Protection After Hepatitis B Vaccine: Results of a 30-Year Follow-up Study and Response to a Booster Dose. J Infect Dis. 2016 Jul 1;214(1):16-22. doi: 10.1093/infdis/jiv748. Epub 2016 Jan 21. Erratum in: J Infect Dis. 2024 Aug 16;230(2):e504. doi: 10.1093/infdis/jiae336. PMID: 26802139.
Le Conseil National du Sida et des hépatites virales (CNS) et l'Agence nationale de recherches sur le sida | Maladies infectieuses émergentes (ANRS | MIE). Traitement préventif post-exposition au VIH. Practice guidelines - Updated on Aug 02 2024. Accesible en: https://www.has-sante.fr/jcms/p_3536535/en/traitement-preventif-post-exposition-au-vih#voirAussi
Documento de consenso Diagnóstico y tratamiento de las infecciones de transmisión sexual en adultos, niños y adolescentes. Noviembre de 2024. Panel de expertos del Ministerio de Sanidad del Gobierno de España y de los grupos de trabajo de la SEIMC, GeSIDA, GEITS y GEHEP. Accesible en: https://seimc.org/contenidos/documentoscientificos/seimc-dc-2024-Documento-ITS-geits-gesida-gehep.pdf
8. PROFILAXIS POSEXPOSICIÓN EN NIÑOS Y ADOLESCENTES
Generalidades
En general la atención de niños, niñas y adolescentes potencialmente expuestos a VIH, VHB o VHC se realizará en servicios de urgencias pediátricos o centros especializados, en los que exista la posibilidad de realizar un abordaje integral de la situación.
Debe informarse al tutor legal de los menores de 16 años de los riesgos de la exposición y los beneficios de la PPE. Los menores capacitados para la toma de decisiones que no deseen que se notifique la situación a un adulto/tutor responsable, y tras valorar riesgos y beneficios, deben ser igualmente atendidos, justificando detalladamente la situación en la historia clínica. En mayores de 16 años no se requiere notificación a tutor legal. En caso de sospecha (o confirmación) de abuso sexual, este debe notificarse a las autoridades judiciales correspondientes y asegurar un examen físico forense por personal adecuadamente formado y acreditado.
Es necesario establecer la necesidad de PPE de forma individualizada. Previo al inicio de la PPE se debe realizar al menos estudio básico, como en población adulta (ver capítulo 7).
Debe ofrecerse el tratamiento para los primeros 3-5 días y asegurar su seguimiento en consultas de enfermedades infecciosas o Infectología Pediátrica de referencia, en ausencia de este recurso lo asumirá la consulta de pediatría general o el centro de referencia de ITS, donde se ofrecerá tratamiento completo, adherencia a PPE y seguimiento posterior. Se recomienda que se disponga de kits de medicación antirretroviral preparados en servicios de urgencias pediátricas o centros de referencia. (BIII)
Las situaciones más habituales en las que se plantea PPE en niños, niñas y adolescentes son:
- El pinchazo accidental con aguja de origen desconocido. Es la situación más habitual en niños y en general no requiere profilaxis posexposición (CIII). Debe iniciarse PPE si el pinchazo se produce con aguja usada recientemente por persona que vive con VIH con carga viral detectable o desconocida o persona que se inyecta droga.
- La mordedura es un motivo frecuente de consulta en niños y niñas. El riesgo de transmisión es muy bajo. Por tanto, en caso de mordedura humana, NO se recomienda profilaxis (CII) salvo que concurran TODAS estas condiciones: saliva contaminada con sangre visible, persona que ha ocasionado la mordedura tenga (o se sospeche) carga viral > 1000 copias/ml y la mordedura haya ocasionado herida profunda.
- Si existe (o se confirma) posibilidad de abuso sexual o si consultan por relación sexual de riesgo (penetración vaginal o recepción anal sin protección) debemos saber que en población pediátrica se asocia mayor riesgo de transmisión viral por mayor vulnerabilidad anatómica a los traumatismos, una mucosa vaginal y anal más fina, ectopia cervical, etc.
Profilaxis VIH
La PPE en el niño y adolescente supone un reto debido a la problemática legal ya que en muchas ocasiones esta se origina después de un abuso o violación, pero también debido a que la disponibilidad de fármacos no es la misma que para el adulto y se tiene que diseñar en base a las formulaciones existentes. Esta debe iniciarse idealmente en las primeras 2 horas, preferiblemente en las primeras 12 horas, y siempre antes de las 72 horas. (AII)
La duración de la profilaxis siempre será de 28 días. La elección del fármaco se hará en función de la edad y peso del paciente, de acuerdo con la Tabla 1 (AII)
Profilaxis VHB
La indicación o necesidad de profilaxis viene determinada por el estado y respuesta vacunal del sujeto expuesto y se detalla en la figura 4.1. del tema 4. En población pediátrica, si existe indicación, la profilaxis consiste en la administración de una dosis de inmunoglobulina anti hepatitis B (0,6 ml/kg; dosis mínima: 0,5 ml; dosis máxima: 5 ml), en las primeras 24 horas o hasta un plazo máximo de 14 días después de la exposición y una segunda dosis al mes en no respondedores a la vacunación. En no vacunados, ésta se iniciará según la pauta estándar (tres dosis: 0, 1 y 6 meses). En menores de 16 años, las dos vacunas disponibles en nuestro medio son: Engerix B JuniorⓇ (10 mcg, GSK) y HBVAXPROⓇ (5 mcg, Sanofi Pasteur MSD).
Profilaxis VHC
No existe profilaxis para el virus de la hepatitis C. Al paciente se le hará seguimiento mediante la determinación de anticuerpos anti VHC como en el adulto.
Tablas:


Bibliografía:
Dominguez K, Smith DK, Vasavi T, et al. Updated guidelines for antiretroviral postexposure prophylaxis after sexual, injection drug use, or other nonoccupational exposure to HIV—United States, 2016. Published Date: April 18, 2016, Update (May 23, 2018). Available: https://stacks.cdc.gov/view/cdc/38856
Title : Updated Guidelines for Antiretroviral Postexposure Prophylaxis After Sexual, Injection Drug Use, or Other Nonoccupational Exposure to HIV—United States, 2016. Personal Author(s) : Dominguez, Kenneth L.;Smith, Dawn K.;Vasavi Thomas,;Crepaz, Nicole;Lang, Karen;Heneine, Walid;McNicholl, Janet M.;Reid, Laurie;Freelon, Brandi;Nesheim, Steven R.;Huang, Ya-lin (Aileen);Weidle, Paul J.; Published Date : April 18, 2016, Update (May 23, 2018) URL : https://stacks.cdc.gov/view/cdc/38856
Panel de Expertos de GeSIDA. Documento de consenso sobre profilaxis postexposición ocupacional y no ocupacional en relación con el VIH, VHB y VHC en adultos y niños. (actualización marzo 2015). Accesible en: https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/hepatitisC/informacion/docs/Profilaxis_postexposicion_ocupacional_y_no_ocupacional_VIH_VHB_VHC(PPE).pdf
Martínez Gómez X, Rodrigo Pendás JA, González Peris S, Sancosmed Ron M, Caballero Requero E, Cabañas Poy MJ, et al. Protocolo de actuación tras pinchazo accidental en niños y adolescentes. Hospital Vall d’Hebron. Marzo 2023. https://www.upiip.com/sites/upiip.com/files/Protocolo%20pinchazo_marzo%202023_0.pdf
WHO. Vaccines and immunization for monkeypox: Interim guidance, 16 November 2022. https://www.who.int/publications/i/item/WHO-MPX-Immunization
Post-Exposure Prophylaxis after non-occupational and occupational exposure to HIV. Australian National Guidelines (Third edition) 2023. Accesible en: https://pep.guidelines.org.au/wp-content/uploads/2023/07/ASHM-PEP-Guidelines_2023_3rd-edition.pdf
Comité Asesor de Vacunas (CAV-AEP). Manual de Inmunizaciones en línea de la AEP [Internet]. Madrid: AEP; 2024. [consultado el 03/11/2024]. Accesible en: http://vacunasaep.org/documentos/manual/cap-9
Villaverde S, Bello P, Rojo P. Pinchazo accidental y otras exposiciones a virus transmitidos por sangre y fluidos corporales (v.4/2019). Guía-ABE. Infecciones en Pediatría. Guía rápida para la selección del tratamiento antimicrobiano empírico [en línea][actualizado el 05/01/2019; consultado el abril 2024]. Disponible en http://www.guia-abe.es
9. SITUACIONES DE NO RECOMENDACIÓN DE PPE
Introducción.
De forma general no se recomienda administrar la PPE si el riesgo de transmisión es muy bajo (< 1 / 10 000) ya que el riesgo de potencial toxicidad e inconveniencia de la PPE seguramente es superior al beneficio, salvo que exista alguna circunstancia específica que aumente el riesgo por encima de > 1 / 10 000 1. Si bien, dada la buena tolerabilidad de los nuevos antirretrovirales y la corta duración de la pauta, existen escasos o nulos riesgos a la hora de administrarla, ésta no debería ser recomendada en aquellas situaciones en las que tampoco se obtendrá ningún beneficio. Basándose en el principio bioético de autonomía, por el cual las personas deben tomar sus propias decisiones libremente una vez informadas, debemos transformar los escenarios clínicos de una “no indicación” del profesional, a una “desestimación” de la estrategia por parte de la persona solicitante. Por ello, toda valoración de PPE requiere tiempo, para poder realizar un asesoramiento adecuado y poder exponer las razones científicas por las que el clínico considera que iniciarla no aportará beneficio, para que sea el solicitante quien pueda tomar una decisión de forma libre. Se debe tener en cuenta que una persona que acude solicitando la PPE, se encuentra en un momento vital que genera estrés puesto que dicha persona considera que puede haber contraído la infección. Es vital entender el proceso que atraviesan y empatizar para poder llevar a cabo un correcto acompañamiento, para evitar la innecesaria medicalización de una situación de miedo, y poder dar respuesta mediante la información y empoderamiento.
Escenarios de no recomendación.
Exposición sexual.
A continuación, se disponen las situaciones en las que generalmente la PPE no está recomendada:
- Relaciones sexuales de cualquier modalidad cuando la pareja sexual tiene VIH y se encuentra en tratamiento y con carga viral indetectable durante al menos 6 meses 23. (AI)
Existen numerosos estudios que demuestran que las personas con VIH y carga viral indetectable NO pueden transmitir la infección (Indetectable = Intransmisible).
- Cualquier práctica sexual (excepto sexo anal receptivo con eyaculación) con parejas sexuales de las que se desconoce el estado serológico y que no pertenecen a poblaciones con prevalencia de VIH > 1 % (personas asignadas hombre al nacer que tienen sexo con hombres, personas que usan drogas inyectadas y realizan intercambio de material, migrantes procedentes de países con alta prevalencia) 1. (BIII)
Basándose en la fórmula para cálculo la probabilidad de transmisión de la infección:
La probabilidad de transmisión en el sexo anal receptivo con eyaculación con personas de poblaciones con prevalencia de VIH > 1 % seria 1 / 6500. En el resto de prácticas la probabilidad sería < 1 / 10000 por lo que no estaría recomendada la PPE.
- Sexo oral tanto insertivo como receptivo con o sin eyaculación en cavidad oral íntegra 4. (BII)
Un estudio observacional realizado en nuestro país en 2002, no evidenció ningún caso de transmisión de VIH tras analizar 19 316 contactos mediante sexo oral entre parejas serodiscordantes sin la utilización de métodos barrera. De éstas, 3 060 fueron actos orales receptivos con eyaculación en cavidad oral.
Se debe tener precaución en circunstancias que puedan aumentar la probabilidad de transmisión debido a la presencia de puertas de entrada en la cavidad oral (aftas orales, mucositis por quimioterapia, intervenciones odontológicas, etc.) y contacto con parejas sexuales con VIH y carga viral elevada (infección aguda).
- Otras: eyaculación en globo ocular, masturbación, besos, prácticas que impliquen contacto piel con piel o contacto con saliva. (AIII)
Exposición ocupacional y otras no sexuales.
- Heridas y salpicaduras con fuente VIH + 5
- De forma general, no se recomienda tras una herida cortante si el caso índice ha permanecido en tratamiento antirretroviral durante, al menos, 6 meses y con carga viral indetectable en este periodo, y que refiera buena adherencia al tratamiento (BII). No obstante, la decisión de tratar se puede considerar de forma individualizada.
- No se recomienda PPE tras una salpicadura si el caso índice mantiene carga viral indetectable de manera sostenida. (AII)
- No se recomienda PPE en situaciones de riesgo de transmisión insignificante, por ejemplo, salpicaduras de sangre u otros fluidos corporales sobre piel intacta. (AII)
- Heridas y salpicaduras con caso índice con estado virológico desconocido 6
No se recomienda PPE tras una herida o salpicadura en mucosas si el caso índice pertenece a un grupo de bajo riesgo. (AIII)
De forma general, no se recomienda PPE tras herida o salpicadura en mucosas si el caso índice pertenece a un grupo de alto riesgo (ej. HSH, UDI), a menos que existan otros factores que incrementen la posibilidad de transmisión (ej. heridas profundas, inyección de sangre o heridas cortantes de un UDI en el contexto de epidemia local). (BIII)
- Pinchazo accidental en ámbito comunitario 7
La PPE no está recomendada. (AIII)
- Mordedura humana 8
De forma general no se recomienda (AIII), salvo que concurran TODAS estas condiciones :
- Saliva contaminada con sangre visible,
- La persona que ha ocasionado la mordedura tiene o se sospecha que tiene carga viral superior a 1000 copias/ml, 3,0 log, y
- La mordedura ha ocasionado una herida profunda
- PPE en personas que se inyectan drogas (UDI) 9
Dado que la prevalencia de infección por el VIH es alta en este colectivo, y que la indicación de PPE es prevenir la transmisión en personas expuestas de forma excepcional y esporádica, no se considera la administración de PPE en UDI que comparten material de venopunción de forma habitual. (BIII)
Bibliografía:
Cresswell F, Asanati K, Bhagani S, Boffito M, Delpech V, Ellis J, et al. UK guidelines for the use of HIV post‐exposure prophylaxis 2021. HIV Med. 2022 May;23(5):494-545. doi: 10.1111/hiv.13208. Erratum in: HIV Med. 2022 Jul;23(6):701. doi: 10.1111/hiv.13327. PMID: 35166004.
Rodger AJ, Cambiano V, Bruun T, Vernazza P, Collins S, van Lunzen J, et al. Sexual Activity Without Condoms and Risk of HIV Transmission in Serodifferent Couples When the HIV-Positive Partner Is Using Suppressive Antiretroviral Therapy. JAMA. 2016 Jul 12;316(2):171-81. doi: 10.1001/jama.2016.5148. Erratum in: JAMA. 2016 Aug 9;316(6):667. doi: 10.1001/jama.2016.10914. Erratum in: JAMA. 2016 Nov 15;316(19):2048. doi: 10.1001/jama.2016.16194. PMID: 27404185.
Cohen MS, Chen YQ, McCauley M, Gamble T, Hosseinipour MC, Kumarasamy N, et al. Prevention of HIV-1 Infection with Early Antiretroviral Therapy.N Engl J Med. 2011 Aug 11;365(6):493-505. doi: 10.1056/NEJMoa1105243. PMID: 21767103; PMCID: PMC3200068.
del Romero J, Marincovich B, Castilla J, García S, Campo J, Hernando V, et al. Evaluating the risk of HIV transmission through unprotected orogenital sex. AIDS. 2002 Jun 14;16(9):1296-7. doi: 10.1097/00002030-200206140-00017. PMID: 12045500.
Cardo DM, Culver DH, Ciesielski CA, Srivastava PU, Marcus R, Abiteboul D, et al. A Case–Control Study of HIV Seroconversion in Health Care Workers after Percutaneous Exposure. N Engl J Med. 1997 Nov 20;337(21):1485-90. doi: 10.1056/NEJM199711203372101. PMID: 9366579.
Cresswell F, Ellis J, Hartley J, Sabin C, Orkin C, Churchill D. A systematic review of risk of HIV transmission through biting or spitting: implications for policy. HIV Med. 2018 Apr 23;19(8):532–40. doi: 10.1111/hiv.12625. PMID: 29687590; PMCID: PMC6120498.
Elósegui López-Quintana ME, Fernández Escribano M, Lucena García S, Mazón Cuadrado L, Orriols Ramos RM, Morais Rodrigues T, et al. Guía de actuación ante exposición ocupacional a agentes biológicos de transmisión sanguínea. Escuela Nacional de Medicina del Trabajo. Instituto de Salud Carlos III. Ministerio de Ciencia e Innovación. Madrid. Actualización 2012. Sánchez Serrano, Sebastián. Coordinador.
Baggaley RF, Boily MC, White RG, Alary M. Risk of HIV-1 transmission for parenteral exposure and blood transfusion: a systematic review and meta-analysis. AIDS. 2006 Apr 4;20(6):805–12. doi: 10.1097/01.aids.0000218543.46963.6d. PMID: 16549963.
Thomas MG, Hopkins CJ, Luey CE. Transmission of HIV infection by severe bites. Int J STD AIDS. 2019 Aug 21;30(9):927–9. doi: 10.1177/0956462419844852. PMID: 31226915.
10. ALGORITMOS, CIRCUITOS DE ACTUACIÓN y ANEXOS
En este capítulo se reúnen un algoritmo general resumido sobre la indicación de PPE, los circuitos de actuación en la PPE ocupacional y no ocupacional, el algoritmo de PPE frente al VHB, un listado de verificación en la PPE, y una tabla simplificada para el seguimiento de personas que reciben PPE. Además, se incluyen como anexos diferentes modelos de hoja de información para la profilaxis posexposición sexual (anexo 1) y hoja de información para la profilaxis posexposición ocupacional (anexo 2).
En opinión de los redactores es suficiente el consentimiento informado verbal, el cuál debe quedar reflejado en la historia clínica del paciente, pudiendo ser válido alguna de estas formas:
1.- “Previo consentimiento verbal del paciente se procede a la toma de muestras para serología frente a VIH, VHB, VHC +/- ITS” (en caso de exposiciones por vía sexual).
2.- “Tras la valoración del riesgo biológico del accidente ocurrido, en base a las Guías de práctica clínica vigentes se recomienda el inicio de profilaxis posexposición (PPE) frente al VIH. La persona que recibirá el tratamiento entiende los riesgos y beneficios de este expresados durante la visita y acepta iniciar PPE”.
Anexo 1. Hoja de información. Profilaxis posexposición sexual.
Antes de empezar:
Es habitual que cuando se tienen relaciones sexuales en las que cabe la posibilidad de haber adquirido el VIH, sobre todo cuando no se ha usado preservativo, se experimenten sentimientos de malestar, ansiedad o culpabilidad.
El preservativo es una herramienta muy eficaz para la prevención del VIH, sin embargo; su uso a veces se puede ver disminuido por múltiples motivos. Durante las relaciones sexuales la capacidad para tomar decisiones puede verse dificultada por presiones, o por la excitación del momento, por ejemplo. Recuerda que nadie debería juzgarte por ello.
Estos pensamientos de culpa que pueden aparecer son comprensibles, pero no te van a hacer bien. Respira hondo 3 veces cuando leas esto, y sé compasivo, compasiva o compasive contigo. Intenta relajarte en la medida de lo posible, acompáñate de gente que te estime y apoye. El sexo es a veces complejo y si no usaste preservativo (de forma consentida) recuerda que estamos aquí para ayudarte sin prejuicios. Disfrutar de una vida sexual placentera es un derecho.
Es por esa dificultad que puede existir a veces para el uso del preservativo que se han desarrollado otras herramientas preventivas como es la profilaxis post-exposición, motivo por el que has acudido.
Es habitual que cuando se tienen relaciones sexuales en las que cabe la posibilidad de haber adquirido el VIH, sobre todo cuando no se ha usado preservativo, se experimenten sentimientos de malestar, ansiedad o culpabilidad.
El preservativo es una herramienta muy eficaz para la prevención del VIH, sin embargo, su uso a veces se puede ver disminuido por múltiples motivos. Durante las relaciones sexuales la capacidad para tomar decisiones puede verse dificultada por presiones, o por la excitación del momento, por ejemplo. Recuerda que nadie debería juzgarte por ello.
Estos pensamientos de culpa que pueden aparecer son comprensibles, pero no te van a hacer bien. Respira hondo 3 veces cuando leas esto, y sé compasivo, compasiva o compasive contigo. Intenta relajarte en la medida de lo posible, acompáñate de gente que te estime y apoye. El sexo es a veces complejo y si no usaste preservativo (de forma consentida) recuerda que no has hecho nada malo. Disfrutar de una vida sexual placentera es un derecho.
Es por esa dificultad que puede existir a veces para el uso del preservativo que se han desarrollado otras herramientas preventivas como es la profilaxis posexposición, motivo por el que has acudido.
¿Qué es la profilaxis posexposición (PPE)?
La PPE es una herramienta preventiva para evitar la infección por VIH cuando se ha tenido una relación sexual en la que puede haberse transmitido. Su pilar fundamental es realizar tratamiento antirretroviral (para el VIH) durante 28 días. Además, durante las visitas te ofrecerán realizar pruebas de ITS; test de embarazo y actualizar algunas vacunas.
¿Qué eficacia tiene?
Es difícil estimar la eficacia de la PPE para evitar la infección puesto que por motivos éticos no se han realizado ensayos clínicos. La transmisión del VIH cuando se tienen relaciones sexuales con una persona con la infección y carga viral detectable es inferior al 1.5 %. La PPE ayuda a disminuir esa probabilidad.
¿Cuánto tiempo tengo para pedir la PPE?
La PPE ha demostrado ser eficaz si se da en las primeras 72 h, pero su eficacia disminuye con el tiempo. Por eso es muy importante administrarla cuanto antes mejor, por lo que, si se puede, es preferible acudir en las primeras 24h.
¿Qué riesgos tiene?
La PPE consiste en la toma de medicación para el VIH. Hoy en día, los tratamientos para el VIH son seguros y tienen pocos efectos adversos. Aunque la mayoría de personas no experimentan efectos secundarios, pueden aparecer molestias digestivas (náuseas, vómitos, dolor abdominal) y también cansancio, insomnio o dolor de cabeza.
¿Y cuándo acabe la PPE?
Una vez finalizado el proceso y descartada la infección pregunta a tu médico por otras alternativas para la prevención del VIH. Si has realizado PPE quizá podría interesarte la profilaxis pre-exposición (PrEP).
Anexo 2. Hoja de información. Profilaxis pospexposición ocupacional.
El riesgo de adquirir el VIH después de una exposición ocupacional a sangre u otros fluidos corporales potencialmente infecciosos (líquido cefalorraquídeo, líquidos serosos, líquido amniótico, semen, secreciones vaginales) de una persona con VIH con carga viral detectable o con sospecha de tenerlo es variable según el tipo de exposición. El riesgo medio de transmisión después de una exposición percutánea es de un 0,3 %. Tras una exposición con mucosas el riesgo se reduce a un 0,09 % y es todavía menor cuando el contacto se produce con piel no intacta.
En las exposiciones de mayor riesgo la PPE puede ser de utilidad, disminuyendo el riesgo de contraer el VIH. La PPE es un tratamiento preventivo que consiste en tomar durante cuatro semanas medicamentos frente al VIH (antirretrovirales) con el objetivo de reducir la probabilidad de adquirir el virus tras haberse expuesto al mismo. Los datos disponibles sugieren que este tratamiento es eficaz en la mayoría de los casos para evitar la infección, aunque se han comunicado fallos del mismo. La PPE se debe iniciar lo antes posible y como máximo hasta 72 horas después de la exposición, no estando indicada si el tiempo transcurrido es mayor. Su eficacia disminuye con el tiempo por lo que es muy importante administrarla cuanto antes, idealmente en las primeras 24 h. Por otra parte, en el momento actual no existe ninguna otra alternativa terapéutica para prevenir la infección por el VIH en esta situación. Si la PPE está indicada sus beneficios superan sus riesgos potenciales.
Los medicamentos antirretrovirales pueden producir efectos secundarios con cierta frecuencia, aunque en general no son graves y se suelen resolver tras finalizar el tratamiento. Los efectos secundarios graves o irreversibles son muy poco frecuentes. Los efectos secundarios más habituales son cansancio, náuseas, vómitos, diarrea, dolor abdominal, flatulencia, dolor de cabeza, insomnio, mareos y dolores musculares. Con menor frecuencia pueden producir reacciones alérgicas, erupciones cutáneas, anemia, alteraciones renales y hepáticas. Los medicamentos antirretrovirales pueden ser incompatibles con otras medicinas, por lo que debe informar al médico de todos los medicamentos que esté tomando. Si usted está embarazada o cree que puede estarlo comuníqueselo al médico. Durante la PPE y posteriormente, durante 4-6 meses, se le realizará un seguimiento periódico en la consulta del especialista. Si tiene alguna duda puede realizar todas las preguntas que considere oportunas.
Gráficos:
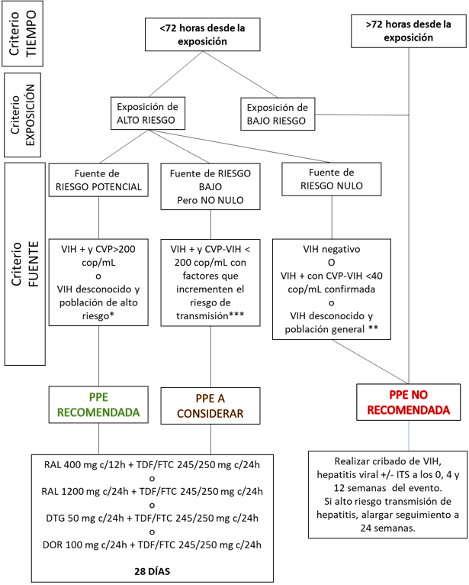


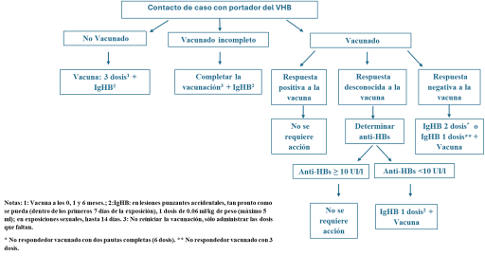
Tablas:

